Перекрёстные ссылки книги для 6. Safety and management of adverse drug reactions in TB preventive treatment

ВОЗ на протяжении многих лет рекомендует проводить ПЛТ среди групп населения, подверженных риску ТБ, в первую очередь – среди ЛЖВ и детей из домашних очагов ТБ инфекции. Однако программное расширение масштабов ПЛТ в большинстве стран с высоким бременем ТБ и ВИЧ остается ограниченным вследствие других конкурирующих приоритетов.
Дополнительными факторами, способными препятствовать такому внедрению, являются опасения по поводу эффективности и безопасности ПЛТ и его взаимодействия с лечением другими препаратами, в первую очередь АРВ. Часто также звучат вопросы о степени вероятности того, что ПЛТ приведет к повышению бремени лекарственно-устойчивого ТБ в конкретном сообществе, и о долгосрочности его эффекта с точки зрения защиты от заболевания ТБ и снижения уровня смертности. В этой главе рассматриваются имеющиеся данные по некоторым из этих важных вопросов, которые могут способствовать популяризации и программному широкомасштабному внедрению ПЛТ
Лекарственная безопасность и нежелательные реакции на лекарственные препараты
В целом нежелательные явления, которые приводили бы к гибели пациента или требовали прекращения ПЛТ, возникают достаточно редко. В то же время очень важно заблаговременно выявлять любые признаки токсического воздействия препарата и оперативно принимать необходимые меры, особенно это касается в целом здоровых людей. Помимо ущерба, который может быть нанесен здоровью человека, подобные события могут негативно отражаться на репутации всей программы и приводить к широкомасштабному приостановлению ПЛТ вследствие утраты доверия к нему в обществе. Как и в случае с любыми другими профилактическими мерами, медработник должен взвешивать все риски и преимущества ПЛТ для каждого конкретного человека. Сбор подробного и точного анамнеза (включая принимаемые лекарственные препараты и известные нежелательные реакции на препараты, возникавшие в прошлом) и обновление данных о людях, получающих ПЛТ, при каждом взаимодействии с ними поможет выявить тех, кто нуждается в постоянном мониторинге, и определить оптимальный порядок действий в случае возникновения нежелательных явлений. В отношении людей, получающих ПЛТ, также важно проводить постоянный мониторинг в форме регулярных визитов (по возможности на ежемесячной основе или в соответствии с предписаниями национальных программ или потребностями конкретного человека).
В таблице 6.1 представлены известные нежелательные явления, связанные с приемом препаратов, в настоящее время назначаемых в рамках ПЛТ. На этапе первичного консультирования медработник должен разъяснить пациенту, как протекает заболевание, обосновать необходимость лечения и подчеркнуть важность получения полного курса терапии, сообщить о возможном возникновении нежелательных явлений и о необходимости обращения в медицинское учреждение при появлении следующих симптомов, свидетельствующих о токсическом воздействии препаратов, в период между визитами: отсутствие аппетита, постоянная усталость или слабость, ощущение дискомфорта в области живота, тошнота, рвота, потемнение цвета мочи, светлый стул, сыпь или зуд, пожелтение кожи или белков глаз, ощущения покалывания или онемения в руках или ногах. Если при возникновении таких симптомов обратиться в медицинское учреждение не удается, то ПЛТ следует немедленно прекратить. Людей, принимающих рифамицины, следует заблаговременно проинформировать о возможном окрашивании физиологических жидкостей в розовый цвет на фоне приема этого препарата.
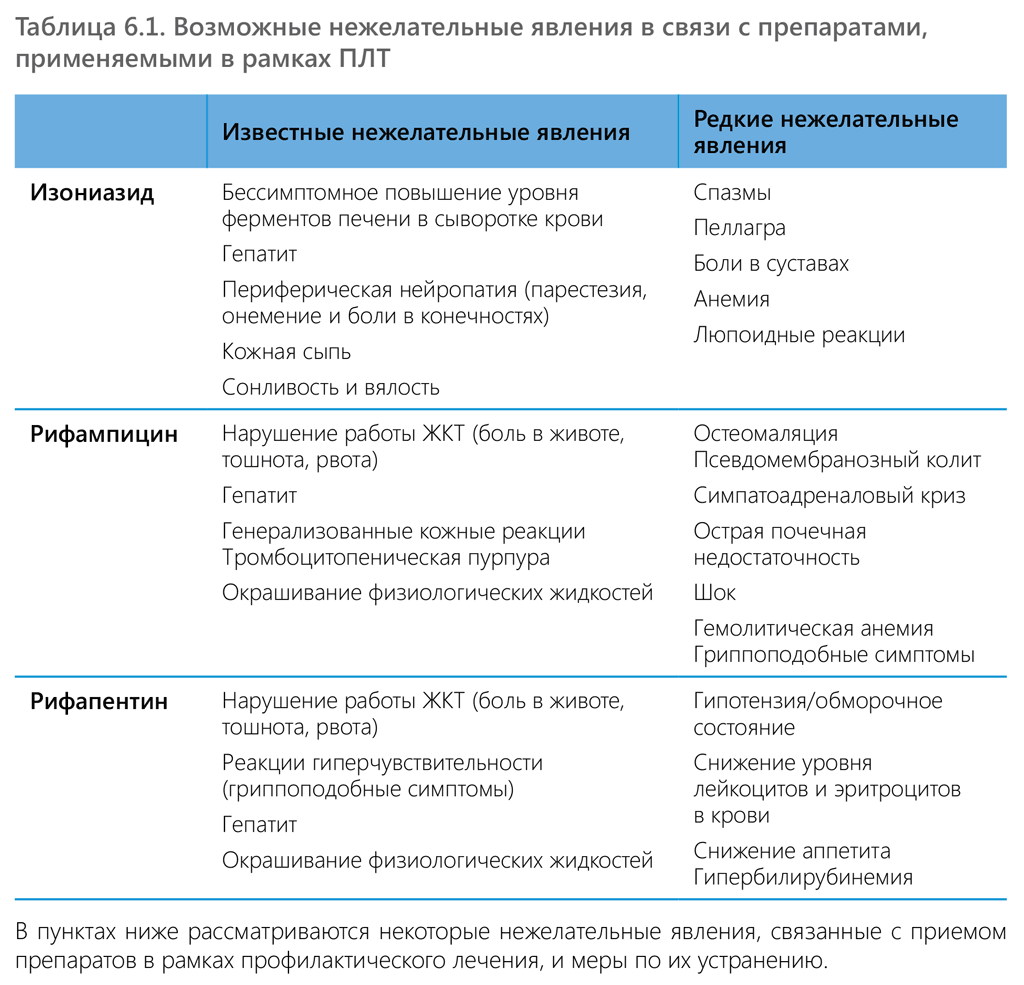
Изониазид
- Бессимптомное повышение уровня ферментов печени в сыворотке крови может возникать у 10–20% людей, принимающих изониазид, и эти показатели обычно возвращаются в норму даже при продолжении лечения. В то же время, в соответствии с общими рекомендациями, прием изониазида следует приостановить в том случае, если уровень трансаминаз превышает верхнюю границу нормы в три раза и при этом наблюдается возникновение симптомов, а также при пятикратном превышении верхней границы нормы даже при отсутствии симптомов.
- Клинический гепатит с летальным исходом возникает у 0,1% пациентов, принимающих изониазид, и чаще всего при сочетании изониазида с другими гепатотоксическими препаратами. К факторам, способным повышать частоту случаев и тяжесть гепатита, относят ежедневное употребление алкоголя, первичные заболевания печени или риск развития заболеваний печени, возраст старше 65 лет и одновременный прием других препаратов, которые метаболизируются в печени. Клинически проявляющийся гепатит редко наблюдается у людей моложе 20 лет, несмотря на то что существуют данные о ряде случаев тяжелого течения заболевания и летальных исходов. Молодые люди, у которых имеются сопутствующие факторы риска развития заболеваний печени, нуждаются в клиническом мониторинге с соблюдением тех же мер предосторожности, которые применяются в отношении пожилых людей.
- Периферическая нейропатия (парестезия, онемение и боли в конечностях) встречается у менее чем 0,2% пациентов, принимающих изониазид в обычной дозировке. Периферическая нейропатия чаще развивается на фоне других заболеваний/состояний, сопутствующих ее возникновению, таких как сахарный диабет, неполноценное питание, ВИЧ-инфекция, почечная недостаточность и алкоголизм. Плановый прием пиридоксина (витамина B6) рекомендован только тем пациентам, у которых наблюдаются подобные нарушения здоровья или которые подвергаются другим рискам токсического воздействия изониазида.
- Изониазид является подтвержденной вторичной причиной развития такого заболевания, как пеллагра. Он препятствует выработке ниацина (витамин B3) на клеточном уровне у людей, которые изначально страдают от дефицита питательных веществ. Ниацин играет очень важную роль во многих процессах обмена веществ. Основанием для постановки диагноза «пеллагра» является такое клиническое проявление, как характерная кожная сыпь. К другим симптомам пеллагры относят диарею и психоневротические расстройства. Повышенному риску развития пеллагры подвержены люди, которые злоупотребляют алкоголем, а также те, чей рацион состоит преимущественно из необработанной кукурузы.
- В числе других известных побочных эффектов приема изониазида – кожная сыпь, сонливость и вялость.
Рифампицин
- Гастроинтестинальные симптомы, такие как тошнота, потеря аппетита и боль в животе, редко носят настолько тяжелый характер, чтобы требовалось прекращение лечения.
- Гепатотоксичность, проявляемая в виде транзиторной субклинической гипербилирубинемии, может возникать у 0,6% пациентов, принимающих рифампицин. Возникновение гепатита более вероятно в случае приема рифампицина в сочетании с изониазидом.
- Кожные реакции, например кожный зуд (с сыпью или без), могут возникать примерно у 6% людей, принимающих рифампицин. Они, как правило, проходят самостоятельно и не всегда свидетельствуют об истинной гиперчувствительности. Лечение при этом может быть продолжено.
- Синдром гиперчувствительности к рифамицину в прошлом наблюдался при использовании рифампицина и характеризовался гриппоподобными симптомами. Этот синдром, как правило, возникает через несколько недель после начала лечения и в большинстве случаев пациенты хорошо переносят последующее лечение ТБ (96, 97). В редких случаях рифамицины могут вызывать реакции гиперчувствительности, включая гипотензию, нефрит и тромбоцитопению, сопровождаемые такими симптомами, как повышение температуры, головная боль, головокружение/предобморочное состояние, мышечно-скелетные боли, точечные кровоизлияния и кожный зуд.
- Окрашивание физиологических жидкостей в оранжевый цвет допустимо и не представляет опасности, однако следует заранее информировать тех, кому назначают рифамицины, о возможности подобной реакции.
Рифапентин
- В целом рифапентин хорошо переносится и вызывает меньшее число нежелательных явлений в рамках ПЛТ, даже если речь идет о пациентах с печеночной дисфункцией разной степени (98).
- Клинически значимые системные реакции, как правило гриппоподобные, наблюдаются примерно у 3,5% людей, находящихся на режиме 3HP, причем в большинстве случаев они носят умеренный характер и проходят в течение суток (99). В то же время системные реакции на препараты должны быть предметом клинического мониторинга и постоянного бдительного контроля. Несмотря на подтвержденные случаи гипотензии или обморочных состояний при режиме 3HP, реакции гиперчувствительности в целом у таких пациентов возникают редко и, как правило, быстро проходят после прекращения приема препарата без каких-либо долгосрочных последствий.
- К другим распространенным побочным эффектам относят окрашивание физиологических жидкостей в оранжевый или красный цвет (не представляет опасности), нарушения работы ЖКТ (такие как тошнота, рвота, потеря аппетита), снижение уровня лейкоцитов и эритроцитов в крови, кожная сыпь, зуд, боли в суставах и покраснение глаз (100).
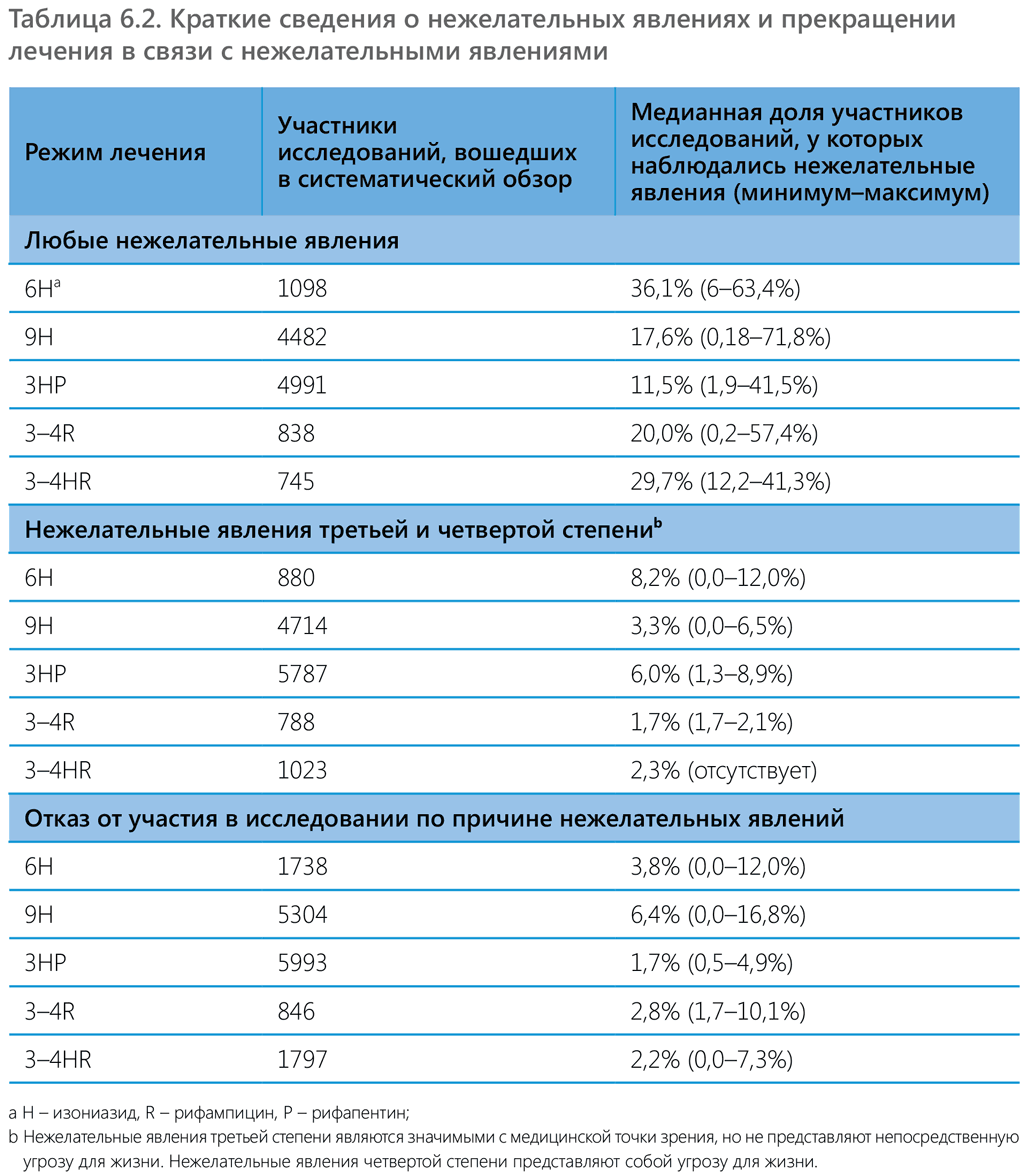
В ходе сетевого метаанализа 2014 г. (обновлен в 2017 г.) производилось сравнение нежелательных явлений, возникавших при стандартном режиме лечения изониазидом и при режимах 3–4R и 3–4HR (45, 101). Было установлено, что режим лечения исключительно рифампицином и режим лечения рифампицином с изониазидом отличаются более низким риском гепатотоксичности по сравнению с монотерапией изониазидом. Еще один систематический обзор 2017 г., включавший данные 23 рандомизированных и 55 нерандомизированных исследований (102), показал, что режим лечения 6H/9H имеет высокие показатели гепатотоксичности (2–6%), тогда как у режимов 3HP и 3–4R эти показатели являются наиболее низкими – 1% и 0,01–2% соответственно (45, 101) (таблица 6.2). В то же время по итогам этого обзора были сделаны четкие выводы в целом о ненадлежащем учете нежелательных явлений, неоднородности данных (использовались разные определения гепатотоксичности) и высоком риске систематической ошибки в исследованиях. Однако полученные данные дали представление о частоте различных нежелательных явлений и реакций, которые в конечном счете приводят к прекращению профилактического лечения. Самые высокие медианные показатели прекращения терапии в связи с возникновением нежелательных явлений были зафиксированы при режиме лечения 6H, за которым следовал режим 9H, а самые низкие значения наблюдались при режиме 3HP. О вероятных реакциях гиперчувствительности сообщили около 4% людей, получавших режим 3HP, и 2% людей с режимом лечения 3HR. Сведений о случаях смерти в период ПЛТ по любым возможным причинам имеется гораздо меньше, и в исследованиях, которые вошли в вышеупомянутый анализ, случаев летального исхода среди участников, получавших режимы 9H, 3HP и 3–4R, зафиксировано не было, тогда как среди тех, кому были назначены режимы 6H и 3–4HR, было несколько случаев смерти, но эти исследования проводились преимущественно среди ЛЖВ, не получавших АРТ или имевших иные сопутствующие заболевания. К счастью, при всех режимах лечения случаи анафилаксии наблюдались крайне редко.
По итогам исследования, в котором сравнивались показатели переносимости режимов 3HP и 9H в группах ВИЧ-положительных и ВИЧ-отрицательных людей, было выявлено, что у ВИЧ-положительных, получавших режим 9H, чаще наблюдались явления токсичности и гепатотоксичности третьей и четвертой степени, а также серьезные нежелательные явления. В то же время доля ЛЖВ, демонстрировавших гриппоподобные симптомы или системные реакции на препараты, оказалась ниже (1,0% по сравнению с 4,6%; P = 0,01) по сравнению с ВИЧ-отрицательными пациентами (53)
 Обратная связь
Обратная связь