Enlaces transversales de Book para 5.1 Recommended TPT regimens
Posologías recomendadas de los fármacos del TPT
El grupo de estudio de la OMS en farmacocinética y farmacodinamia analizó la evidencia disponible a partir de ensayos clínicos de la rifapentina y propuso una posología simplificada de 3HP y 1HP para diferentes franjas de peso, como se resume en el cuadro 5.2 (actualización del 2020 de las directrices). En el cuadro 5.2 se presenta la posología habitual de los esquemas de TPT recomendados, según la edad y el peso corporal.
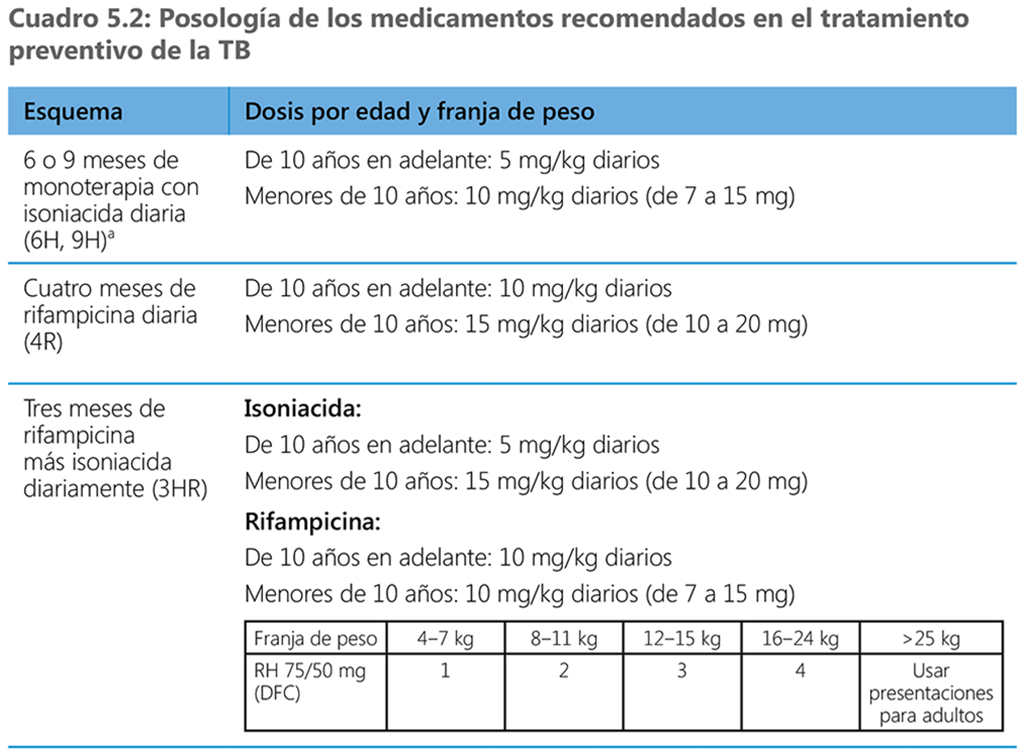
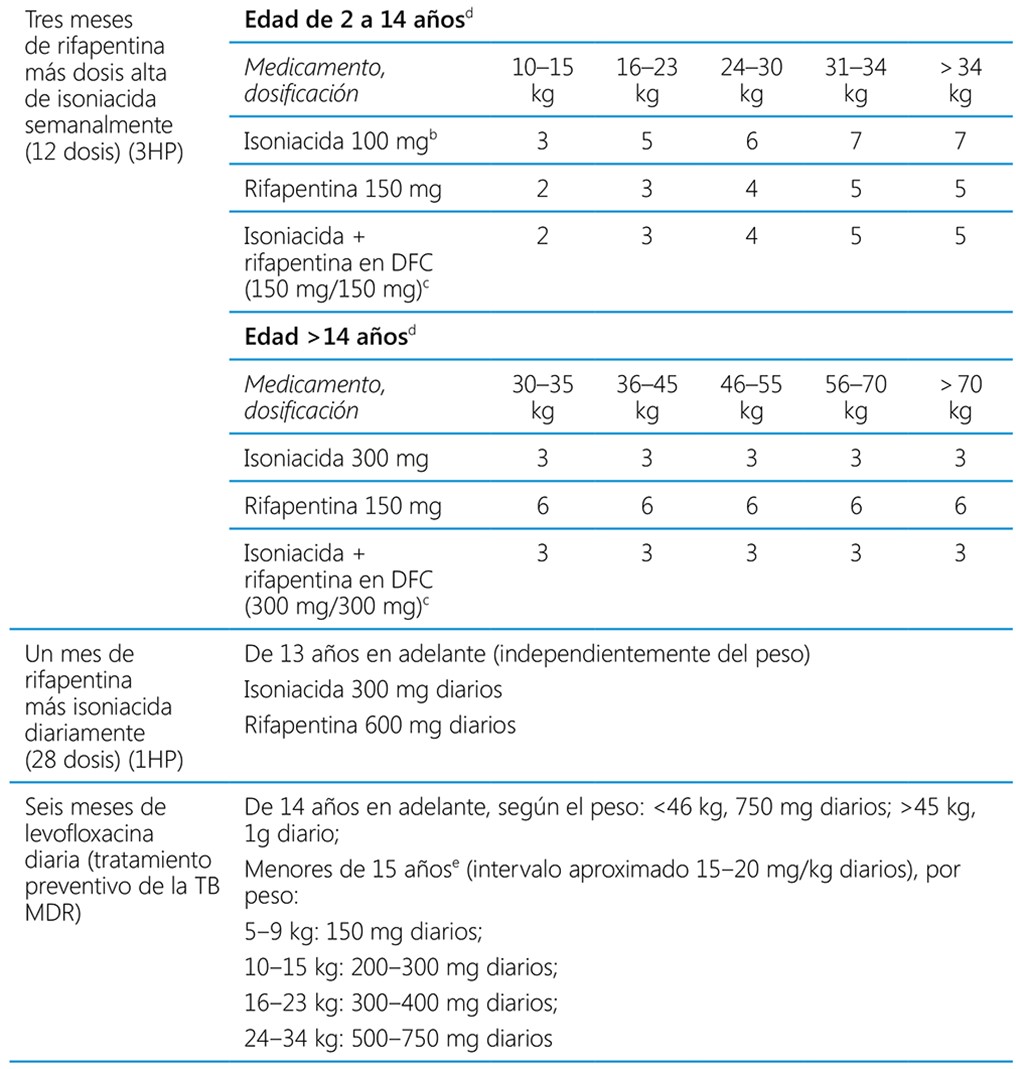
a Un comprimido de la combinación triple que contiene isoniacida 300 mg + piridoxina 25 mg + sulfametoxazol 800 mg + trimetoprim 160 mg (ranurado) es el esquema opcional preferido para personas con infección por el VIH en quienes se piensa administrar una monoterapia con isoniacida (1 comprimido diario para adultos, la mitad del comprimido para niños mayores de 5 años y un cuarto para menores de 5 años).
b Se puede usar la presentación de 300 mg para disminuir el número de comprimidos.
c Se prevé que estará disponible en un futuro próximo
d La posología puede variar en adultos y niños en las franjas de peso superpuestas.
e Están disponibles comprimidos dispersables de 100 mg de levofloxacina para niños.
Los esquemas que contienen isoniacida y rifampicina pueden utilizarse en personas de todas las edades, sin embargo no existen o son muy limitados los datos farmacocinéticos sobre la eficacia para fundamentar la posología apropiada y la seguridad de rifapentina en menores de 2 años y, por lo tanto, el esquema de 3HP solo se recomienda en niños de 2 años en adelante. Además, los datos del ensayo con 1HP se refieren solo a personas a partir de los 13 años de edad. Por consiguiente,aún no se ha establecido la posología diaria de rifapentina apropiada en los menores de 13 años y se deberá examinar la idoneidad de 1HP para este grupo etario cuando se disponga de datos de estudios farmacocinéticos y de seguridad en niños.
Disponibilidad de las presentaciones apropiadas
Rifampicina: Dado el uso generalizado de DFC que contienen rifampicina en el tratamiento de la TB farmacosensible, el uso de dosis simples de rifampicina es menos común, de ahí que su adquisición sea menos frecuente y, por lo tanto, es probable que los programas nacionales dispongan solo de cantidades limitadas. Además, en la actualidad no se cuenta con presentaciones de rifampicina en dosis simple dispersables que sean adaptadas a los niños. Si el esquema preferido es el de 4R, la demanda de comprimidos sueltos de rifampicina aumentará y los programas tendrán que encontrar proveedores de rifampicina en dosis simple de calidad garantizada. La administración de rifampicina también tendría que reglamentarse y limitar su uso como parte del esquema de TPT, sin desviarla para una utilización como un antibiótico de amplio espectro. Los suministros de 4R a los centros periféricos (centros de atención primaria, programas contra el VIH) se deberían aunar a una orientación gradual sobre el uso específico de la rifampicina.
Isoniacida más rifampicina en DFC: Las DFC de 3HR dispersables adaptadas a los niños están disponibles y ya se utilizan en muchos países en el tratamiento de la TB activa en la población infantil. Las mismas presentaciones se pueden utilizar en el TPT. Se deberían preferir las DFC adaptadas a los niños a los comprimidos individuales, con el fin de disminuir la cantidad de pastillas. Del mismo modo, las DFC utilizadas en el tratamiento de la TB activa del adulto, se pueden utilizar en el TPT de los adultos.
Isoniacida más rifapentina (semanal o diariamente): La única presentación de rifapentina actualmente disponible es el comprimido simple de 150 mg. La carga de comprimidos tanto del esquema de 3HP como del de 1HP en los adultos es muy alta. Ya comenzó el desarrollo de DFC de 3HP (con una proporción de rifapentina e isoniacida de uno a uno) y es probable que esté disponible en el 2020. Esto reducirá de nueve a tres el número de comprimidos del 3HP en los adultos. Asimismo, se está desarrollando un comprimido simple de 300 mg de rifapentina, que también podría estar disponible en el 2020, para disminuir a solo tres comprimidos la dosis de 1HP. De igual manera, cuando se cuente con presentaciones en DFC de 3HP (150 mg/150mg) adaptadas a los niños, disminuirá el número de comprimidos en cada dosis. Las futuras investigaciones encaminadas a definir la posología apropiada de rifapentina y evaluar las interacciones medicamentosas (como dolutegravir) en los menores de 2 años, tanto con el 3HP como el 1HP facilitarán la utilización del esquema de 3HP y de 1HP en este grupo etario
Combinación de isoniacida + cotrimoxazol + piridoxina: se puede obtener a precio con descuento por conducto del GDF de la Alianza Alto a la Tuberculosis. Estos comprimidos combinados se pueden considerar como una opción en las personas con infección por el VIH cuando: no se cuenta con esquemas acortados que contienen rifamicina, se presentan interacciones medicamentosas o durante la ampliación gradual de utilización. Se trata de comprimidos con una ranura. Por consiguiente, si la dosis necesaria es un tercio de la presentación para adultos, esta DFC no se puede usar en los menores de 5 años con infección por el VIH
Importancia de la piridoxina y su disponibilidad
Piridoxina (B6): Uno de los efectos secundarios indeseables del tratamiento a largo plazo con dosis altas de isoniacida es la neuropatía periférica que aparece debido a una carencia de vitamina B6 (piridoxina) durante el tratamiento. Las personas con desnutrición, dependencia crónica del alcohol, infección por el VIH, insuficiencia renal o diabetes o las embarazadas y las mujeres que amamantan, corren el riesgo de presentar neuropatía periférica y deberían recibir suplementos de vitamina B6 cuando siguen un esquema que contiene isoniacida. Además, las mujeres durante el embarazo y el puerperio y los lactantes que reciben exclusivamente leche materna deberían recibir vitamina B6 cuando toman isoniacida. La posología habitual de piridoxina cuando se usa como profilaxis de la neuropatía en pacientes que toman isoniacida es de 10 a 25 mg diarios. La neuropatía periférica es infrecuente en otros pacientes que reciben dosis habituales de isoniacida; esta reacción se reconoce fácilmente (por adormecimiento y hormigueo simétricos de las extremidades) y suele ser fácilmente reversible cuando se retira la isoniacida y se inicia un tratamiento con dosis altas de piridoxina (100-200 mg diarios). Por consiguiente, es probable que no sea necesario administrar de manera sistemática suplementos de piridoxina con la is
La piridoxina se convierte in vivo en coenzimas que desempeñan una función esencial en el metabolismo de proteínas, carbohidratos, ácidos grasos y otras sustancias, incluidas las aminas cerebrales. Al parecer, la isoniacida inhibe por competición la actividad de la piridoxina en estas funciones metabólicas (59). La incidencia de neuropatía periférica guarda una estrecha relación con la dosis de isoniacida utilizada. En estudios realizados en la década de 1950 (60-62), se comunicó que si bien una gran proporción (>40%) de las personas que recibían isoniacida en dosis alta (16-24 mg/ kg diarios) presentaba signos y síntomas de neuropatía periférica, solo en 2% de las personas que recibían de 4-6 mg/kg diarios aparecía la neuropatía. La isoniacida en dosis alta puede ser pertinente en el tratamiento de determinadas formas de TB, pero en el TPT se utiliza la dosis habitual de isoniacida. Los signos de toxicidad aparecen mucho más tarde en las personas que reciben dosis inferiores de isoniacida. El síntoma más temprano suele ser la parestesia, seguida de dolor punzante y sensación de ardor en los pies y luego en las manos (adormecimiento y hormigueo simétricos). Si no se tratan, los síntomas empeoran y causan angustia. Es fácil reconocer estos síntomas, que suelen ser reversibles al retirar la isoniacida e iniciar el tratamiento con piridoxina
La administración sistemática de suplementos de piridoxina a personas por lo demás sanas que reciben una dosis habitual de isoniacida tal vez no esté justificada ni sea ni sea obligatoria (62). Sin embargo, incluso las dosis bajas de isoniacida pueden producir neuropatía en los pacientes malnutridos (hasta 20%) (63) y en los acetiladores lentos de la isoniacida7 (hasta un 20% con 4-6 mg/kg de isoniacida). Se sabe que otras personas tienen un riesgo mayor de presentar neuropatía periférica, como las que tienen alcoholismo crónico, infección por el VIH, insuficiencia renal o diabetes y las mujeres durante el embarazo o la lactancia. La administración simultánea de piridoxina con la isoniacida protege contra la aparición de neuropatía periférica en estas personas.
Una alimentación humana adecuada que contenga mezclas de 1 a 2 mg de vitamina B6 al día puede proteger contra la toxicidad de la isoniacida. Las buenas fuentes alimentarias de vitamina B6 son las zanahorias, la espinaca, los guisantes, las papas, la leche, el queso, los huevos, el pescado, la carne y la harina enriquecida. De lo contrario, se puede dar una dosis baja diaria de 10 a 25 mg de piridoxina junto con el TPT a las personas con riesgo alto. La piridoxina se puede administrar en forma de suplementos de vitaminas del complejo B, sobre todo a las personas que pueden tener carencias de otras vitaminas. En el caso de una neuropatía periférica inducida por isoniacida ya establecida, debería administrarse piridoxina en una dosis terapéutica más alta de 50-75 mg diarios e incluso hasta 100 mg o 200 mg por día (64). Es importante mantener la administración de suplementos de piridoxina en la dosis adecuada, porque las concentraciones más altas pueden interferir con la actividad antimicobacteriana de la isoniacida. Además, se ha informado que dosis excesivamente altas de piridoxina, de 2000 mg diarios o más, causan toxicidad, incluso neuropatía periférica (65-67).
Actualmente, la presentación de piridoxina disponible por conducto del Mecanismo de Adquisiciones Conjuntas del Fondo Mundial y la lista de productos del GDF son comprimidos de 50 mg sin recubrimiento y comprimidos recubiertos de 100 mg (51). Ambas presentaciones son adecuadas principalmente para uso terapéutico y son difíciles fraccionar para la posología recomendada como suplemento profiláctico. Los programas nacionales pueden considerar la posibilidad de adquirir localmente un producto de calidad garantizada de piridoxina en dosis más bajas (10-25 mg) para su uso en personas de alto riesgo o bien adquirir vitaminas del complejo B. En las personas con infección por el VIH se puede considerar la posibilidad de utilizar el comprimido combinado de isoniacida + B6 + cotrimoxazol. No obstante, también se recomienda que los programas almacenen piridoxina en dosis más altas (que se puede obtener por conducto de la lista de productos del GDF) para el tratamiento de la neuropatía periférica.
Mensaje clave: Durante la ampliación de los servicios de TPT, la falta de piridoxina no debe convertirse en un obstáculo al inicio del TPT. Se debe emprender la evaluación clínica del riesgo de neuropatía antes de recetar suplementos de piridoxina.
Introducir y ampliar la ejecución del TPT
Consideraciones relativas a la ejecución programática del TPT
- Definir las funciones y las responsabilidades de los cuadros de trabajadores de salud para recetar el TPT. Miembros capacitados del personal médico, de enfermería y trabajadores periféricos de atención de salud pueden evaluar y comenzar el TPT una vez que se descarte de manera fiable la TB, siguiendo el protocolo nacional. También se puede capacitar al personal de enfermería y los trabajadores de salud de primera línea en la periferia para supervisar el TPT y tomar decisiones en materia de suspensión o modificación del TPT (por ejemplo, en el caso de eventos adversos) o su reanudación (por ejemplo, después de una interrupción por parte de la persona tratada). En la mayoría de los casos no hay necesidad de buscar opinión médica o de un especialista al tomar estas decisiones; sin embargo, deberían adoptarse medidas que permitan obtener este apoyo en caso de que sea necesario.
- Definir los niveles del sistema de atención de salud donde se puede iniciar el TPT y reponer los medicamentos para su continuación
- Elaborar los procedimientos estandarizados de trabajo para la iniciación y el seguimiento del TPT, con el fin de:
- mantener flujo de personas que deben recibir el TPT en distintos establecimientos de salud y en los diferentes puntos de servicio en estos establecimientos;
- determinar la función y las responsabilidades de los trabajadores de salud, los agentes comunitarios de salud y los interesados directos clave (como los servicios de atención de la desnutrición, las prisiones, los establecimientos correccionales, los campamentos de refugiados o las comunidades de minería) en la evaluación de los criterios de selección para recibir el TPT y el comienzo del mismo;
- prestar apoyo en materia de adhesión al TPT;
- gestionar las interrupciones del TPT; y
- detectar, documentar y manejar los eventos adversos a los medicamentos.
- Establecer servicios de TPT en todos los centros de prestación de servicios pertinentes (como los centros de tratamiento de la TB, los centros de TAR, los centros de atención de la salud maternoinfantil o los centros de salud comunitaria).
- Descentralizar hacia los centros de TB que suministran TAR o tratamiento contra la TB (iniciación y continuación) más cercanos a la residencia de la persona, con el fin de reducir al mínimo el tiempo de desplazamiento para recibir el TPT
- Aprovechar los servicios existentes de TB, VIH y de salud general para prestar la atención especializada necesaria a las personas que reciben el TPT (como el manejo de los eventos adversos, las interacciones medicamentosas y las situaciones especiales [embarazo]).
- Evaluar la capacidad y la disponibilidad de trabajadores de salud y estimar las necesidades adicionales para ampliar a escala nacional los servicios de TPT.
- Evaluar la disponibilidad y la capacidad de los agentes comunitarios de salud y otras redes (como los antiguos pacientes con TB) que puedan contribuir a la prestación de servicios de TPT y el apoyo a las personas.
- Creación de capacidad:
- mediante la capacitación inicial, la concientización y el fortalecimiento de la capacidad del personal;
- de los médicos de atención primaria, el personal de enfermería y otros trabajadores de salud, en la elaboración de la historia clínica, el tamizaje por los síntomas y la derivación para investigaciones complementarias, la evaluación de los criterios de aptitud para recibir el TPT y el inicio del mismo; y
- de los agentes comunitarios de salud en la provisión y el seguimiento del TPT.
- Emprender la planificación de la introducción y el retiro de los medicamentos del TPT (desde la perspectiva de las adquisiciones) a medida que el programa nacional evoluciona hacia los esquemas acortados de TPT. Este aspecto es importante durante la introducción del nuevo esquema.
- Examinar y fortalecer el mecanismo de cuantificación, solicitud y suministro ininterrumpido de productos básicos (como los medicamentos del TPT o la piridoxina).
- Abordar aspectos específicos del TPT para los niños, con el fin de:
- coordinar el TPT con varios hogares de miembros de la familia (padres o abuelos), ya que los niños pueden recibir atención en múltiples centros de prestación de servicios (como servicios de salud maternoinfantil, TB o de VIH);
- crear capacidad para el asesoramiento y las medidas en caso de vómito posterior a la ingestión de los medicamentos y las indicaciones para repetir la dosis; y
- suministrar información sobre los alimentos que enmascaran el sabor de los comprimidos.
- Fortalecer el registro y la notificación sistemáticos, incluida la información a partir del formulario de los casos o, alternativamente, la captura de datos en plataformas electrónicas. Es necesario integrar las variables de datos clave en el sistema nacional de información para la gestión de la salud, con fines de seguimiento y evaluación del desempeño.
Iniciación del TPT y evaluación en la línea de base antes de iniciar el TPT
Una vez que se ha descartado la TB activa y se decide considerar la posibilidad de iniciar el TPT, se debe emprender la evaluación de base, a fin de determinar la aptitud de la persona para iniciar el TPT. Esta evaluación abarca los antecedentes personales y de medicamentos y las investigaciones, en conformidad con las directrices nacionales
- Antecedentes personales: obtener la información pertinente para el inicio del TPT y su continuación, como
- alergia o hipersensibilidad conocida a fármacos contra la TB (isoniacida, rifampicina, rifabutina o rifapentina);
- situación frente a la infección por el VIH y esquema de TAR;
- estado de embarazo o método de anticoncepción empleado;
- comorbilidad: evaluar la presencia de afecciones concomitantes (como desnutrición, diabetes o hepatitis viral) y registrar los medicamentos que se toman;
- contactos de pacientes con TB farmacorresistente (isoniacida, rifampicina exclusiva o TB-MDR); y
- posibles contraindicaciones al TPT: como la hepatitis activa (aguda o crónica) o un aumento conocido de las transaminasas (más de tres veces por encima del límite superior normal),consumo regular y excesivo de alcohol y síntomas de neuropatía periférica. Estas afecciones deben dar lugar a investigaciones detalladas y exigen del juicio clínico para sopesar los daños y los beneficios del TPT y el momento para iniciar el TPT cuando los beneficios superan a los daños. Los antecedentes de tratamiento contra la TB o el embarazo actual no deben considerarse como contraindicaciones para iniciar el TPT
- Antecedentes de medicamentos: averiguar los antecedentes de toma de medicamentos con el fin de orientar la elección del esquema de TPT o determinar la necesidad de modificación del tratamiento de las afecciones coexistentes. Ciertas clases de medicamentos como los ARV, los opioides o los antimaláricos a menudo alteran el TPT
- Pruebas de función hepática: no se cuenta con evidencia suficiente que respalde la práctica obligatoria o sistemática de pruebas de función hepática antes del tratamiento (68); es muy posible que el beneficio del TPT sin pruebas hepáticas sea superior a los daños, sobre todo con el uso de esquemas menos hepatotóxicos. Sin embargo, cuando sea factible, se recomienda firmemente realizar pruebas de base en las personas que tienen factores de riesgo, como antecedentes de hepatopatía, consumo regular de alcohol, hepatopatía crónica, infección por el VIH, edad superior a 35 años y embarazo o durante el período del posparto inmediato (los primeros 3 meses después del parto). En las personas con resultados anormales de las pruebas iniciales de función hepática, se requiere un criterio clínico sólido para determinar si el beneficio del TPT supera el riesgo de eventos adversos. En estas personas se deben repetir las pruebas de manera sistemática en las visitas posteriores
Punto clave: Las pruebas sistemáticas de la función hepática no son necesarias antes de comenzar el TPT. La evidencia disponible indica que un seguimiento clínico meticuloso de los signos y los síntomas de hepatopatía es suficiente para la detección temprana y el manejo de los eventos adversos, especialmente con un esquema acortado de TPT que contenga rifamicina. Sin embargo, estas pruebas se recomiendan en las personas que presentan otros factores de riesgo.
- La situación social y económica: de la persona y la familia se debe evaluar y prestar el apoyo necesario con el fin de superar los obstáculos encontrados a la finalización del TPT.
- Asesoramiento:
- Explicar a la persona que reúne los criterios para recibir el TPT y transmitirle los mensajes clave, así como a su familia y a la persona de apoyo al tratamiento, acerca de:
- la justificación del TPT y los beneficios que este aporta a la persona, el hogar y la comunidad en general;
- la disponibilidad del TPT en forma gratuita en el marco de los programas nacionales;
- el TPT que se receta, incluida su duración, las direcciones para la toma de los medicamentos y el plan de seguimiento;
- los posibles efectos secundarios y eventos adversos y qué hacer en caso de que se presenten diferentes efectos secundarios;
- la importancia de completar todo el ciclo de TPT; y
- las razones y el calendario del seguimiento periódico, clínico y de laboratorio, para la supervisión del tratamiento; y
- los signos y los síntomas de TB e indicar los pasos a seguir en caso de que se presenten.
- Acordar el mejor método para apoyar la adhesión al tratamiento, incluido el lugar más conveniente para la toma de medicamentos y el apoyo al tratamiento en función de las preferencias individuales. Se pueden abordar las siguientes opciones:
- Ubicación: el hogar, la comunidad o un establecimiento de salud (con apoyo en forma de orientación).
- Persona de apoyo al tratamiento: evaluar si es necesario designar una persona que provea el tratamiento o si es posible la autoadministración. Cuando se precisa una persona de apoyo al tratamiento, se puede tratar de una persona que ha recibido orientación como un miembro de la familia, un voluntario de la comunidad, un colaborador con el tratamiento en el lugar de trabajo o de un trabajador de salud. En el caso de un esquema semanal, es preferible que la ingesta de cada dosis sea observada directamente por el familiar, el miembro de la comunidad o el colaborador con el tratamiento en el lugar de trabajo que han recibido orientación, o por el trabajador de salud (ya sea en persona o mediante una herramienta digital)
- Herramientas digitales: incluyen el tratamiento observado por video, las llamadas telefónicas perdidas o los recordatorios por servicios de mensajes cortos (SMS).
- Explicar a la persona que reúne los criterios para recibir el TPT y transmitirle los mensajes clave, así como a su familia y a la persona de apoyo al tratamiento, acerca de:
Adhesión
La adhesión al ciclo del TPT y la finalización del tratamiento son factores determinantes importantes del beneficio clínico, tanto a escala individual como de la población (capítulo 7). Un tratamiento irregular o inadecuado disminuye la eficacia protectora del esquema de TPT. Además, una adhesión precaria o la cesación temprana del TPT puede aumentar el riesgo evolución hacia la TB, incluso la TB farmacorresistente (aunque no está respaldado por la evidencia científica disponible). Se sabe que la mayor eficacia del TPT se logra cuando se toma al menos 80% de las dosis en el plazo de duración del esquema. El número total de dosis tomadas es también un determinante clave de la magnitud de la prevención de la TB (69,70).
En los ensayos clínicos han usado varias definiciones de finalización del ciclo de tratamiento preventivo, a saber: 80% de las dosis recomendadas, consumidas en el 120% de la duración planificada del TPT (71) o 90% de las dosis recomendadas consumidas en el 133% de la duración prevista (72). En el cuadro 5.3 abajo se resumen todos los esquemas recomendados y los criterios sugeridos para evaluar la finalización de los diferentes esquemas. Es de esperar que los esquemas acortados se asocien con una mejor adhesión y una tasa más alta de finalización del tratamiento
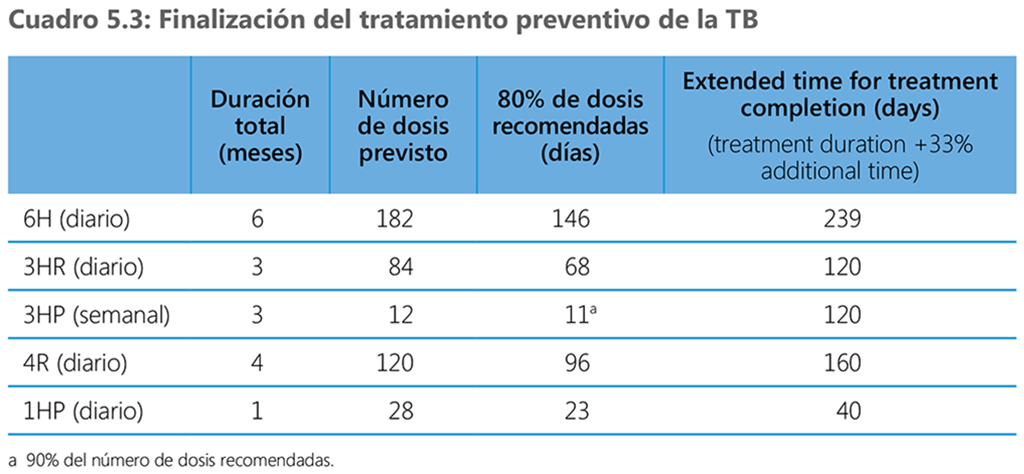
a 90% del número de dosis recomendadas.
Los programas nacionales deben adaptar los mecanismos para mejorar la adhesión a las necesidades específicas de los grupos en riesgo y al contexto local del país. En general, una autoadministración eficaz es posible con todas las opciones de TPT. Es poco probable que el TPT aumente el riesgo de selección de micobacterias farmacorresistentes, al contrario de lo que ocurre con el tratamiento de la TB. La modalidad del suministro del tratamiento y del apoyo a la adhesión se debe determinar en primer lugar en función de las preferencias de la persona. Las directrices de la OMS sobre el TPT del 2015 revelan resultados heterogéneos y una evidencia no concluyente con respecto a las intervenciones para mejorar la adhesión al tratamiento y fomentar la finalización (73). Sin embargo, el recuento de comprimidos por parte de los prestadores de atención en cada contacto con la persona que recibe TPT es de bajo costo y factible y en un ensayo clínico se demostró que tiene un excelente valor pronóstico sobre la reducción del riesgo de contraer la TB (69); esta medida debería incorporarse en todos los servicios de TPT. Además, la adquisición de productos en envases alveolados o blisters puede facilitar una mejor supervisión de la adhesión, en comparación con los frascos de comprimidos
Las directrices de la OMS sobre el tratamiento de la TB farmacosensible proponen varias intervenciones de apoyo a la adhesión que también podrían aplicarse al TPT (74). Entre ellas figuran las redes de apoyo entre pares, las intervenciones educativas y de orientación personalizada que incluyan un asesoramiento de buena calidad y el tratamiento observado por video. Los programas nacionales deberían destinar recursos económicos y humanos suficientes para fortalecer los mecanismos de adhesión al TPT y no permitir que preocupaciones sobre la adhesión o la falta de herramientas para la adhesión se conviertan en un obstáculo para la ampliación de los servicios de TPT
Gestión de las interrupciones del tratamiento: No existen recomendaciones fundamentadas por la evidencia sobre la gestión de la interrupción del TPT, es decir, cuántas dosis perdidas pueden compensarse prolongando el tratamiento sin afectar su eficacia. En el capítulo 7 se resumen las medidas recomendadas para manejar las interrupciones del tratamiento preventivo, con base en la definición indicativa propuesta arriba de finalización del tratamiento preventivo. Los programas nacionales pueden optar por una definición más o menos estricta de finalización del tratamiento (90% de las dosis recomendadas tomadas en el 120% de la duración planificada del tratamiento, 80% de las dosis recomendadas en el 133% de la duración prevista o una combinación de ambas).
Además de supervisar la finalización del tratamiento (véase también el capítulo 8), se sugieren varios resultados desfavorables que podrían utilizarse para desencadenar una revisión del manejo del caso y, en algunas ocasiones, modificar el tratamiento (véase la lista abajo).
- Fracaso: progresión hacia la TB en cualquier momento durante el TPT.
- Muerte: muerte por cualquier motivo durante el TPT.
- Pérdida durante el seguimiento: TPT interrumpido por la persona durante ocho semanas consecutivas o más en el caso de 6H, cuatro semanas consecutivas o más en el caso de 3HP, 3HR y 4R y 10 días consecutivos con el 1HP.
- Interrupción del TPT debido a la toxicidad: determinada por el médico, debido a eventos adversos o interacciones medicamentosas, con o sin reanudación o cambio del esquema.
- No evaluado: en el caso de registros perdidos, traslado a otro establecimiento de salud con registro de finalización del TPT.
Seguimiento y apoyo durante el TPT
Es necesario dar seguimiento a las personas que reciben TPT en cada contacto con los prestadores de atención de salud. Esto puede hacerse al menos mensualmente o con mayor frecuencia, según lo requiera la atención a las personas en TPT o según el mandato de la política nacional. Se puede capacitar al personal de enfermería y otros trabajadores de salud de primera línea en la periferia para que supervisen y decidan si es necesario modificar el TPT debido a eventos adversos o reiniciarlo (por ejemplo, después de una interrupción por parte de la persona que recibe el tratamiento). No es necesario contar sistemáticamente con una opinión médica o de un especialista para tomar estas decisiones, pero sus servicios deben estar disponibles cuando sea necesario
Otra posibilidad consiste en armonizar el seguimiento con los mecanismos del modelo diferenciado de prestación de servicios dirigido a las personas con infección por el VIH donde se ha introducido o con el calendario de recogida de otros medicamentos (como los ARV). Por principio, el calendario de las visitas de seguimiento o de recogida de medicamentos debe tener en cuenta en primer lugar la conveniencia para la persona. Es importante que se respete una decisión fundamentada de la persona de no aceptar el TPT que se le ofrece o de interrumpirlo después de haberlo iniciado; las personas no deben sentirse obligadas a tomar el tratamiento (véanse también los principios éticos en el capítulo 9). Durante cada contacto con la persona que sigue el TPT, el prestador de atención debe:
- reforzar la comprensión que tiene la persona de los síntomas de la TB, las razones del TPT y la importancia de completar el ciclo;
- comprobar la presencia de signos o síntomas de TB; y en el caso de diagnosticar la TB, debe interrumpirse el TPT y comenzar un tratamiento curativo de la enfermedad;
- medir el peso, si es posible, y ajustar la posología en consecuencia. Esto tiene una importancia particular en los niños pequeños, ya que normalmente puede ocurrir un aumento rápido de peso en los lactantes y los niños pequeños en crecimiento durante el período del TPT, que exige un ajuste de la dosis. Por otra parte, la pérdida de peso documentada o la falta de crecimiento son indicadores clínicos tempranos de TB;
- comprobar la presencia de reacciones adversas, tratar toda toxicidad observada o, de ser necesario, remitir para atención especializada;
- recordar a la persona que sigue el TPT la necesidad de ponerse en contacto con un trabajador de salud o un prestador de atención si observa efectos adversos como anorexia, náuseas, vómitos, malestar abdominal, fatiga persistente o debilidad, orina de color oscuro, heces claras o ictericia; estas manifestaciones son indicadores de lesión hepática y exigen una evaluación urgente; si no fuera posible consultar a un prestador de atención de salud al comienzo de estos síntomas, se debe aconsejar a la persona que suspenda de inmediato el TPT;
- investigar las razones de toda omisión de dosis y extender el apoyo necesario para facilitar el cumplimiento futuro del TPT;
- continuar el tratamiento de las afecciones coexistentes y consultar con el médico a cargo del tratamiento cuando sea necesario;
- preguntar sobre el embarazo, la lactancia materna y el uso de métodos anticonceptivos; y
- tomar nota de la visita, la ingesta de los medicamentos y los hallazgos utilizando la información de los archivos del caso individual o los formularios establecidos por el programa nacional.
Punto clave: En cada oportunidad, los proveedores del TPT deben recordar a quienes lo reciben los posibles eventos adversos y hacer hincapié de nuevo en los signos y los síntomas que deben alertarlos para ponerse en contacto con el trabajador de salud, suspender el TPT o ambas cosas.
Modelo diferenciado de prestación de servicios relacionados con el VIH y sus implicaciones en la ampliación del TPT
Los países con una carga alta de infección por el VIH, en especial en África subsahariana, utilizan cada vez más la prestación diferenciada de servicios de VIH. Estos modelos de prestación dirigidos a los usuarios de la atención de la infección por el VIH que son estables, utilizan un enfoque centrado en la persona y procuran reorientar a las personas que obtienen buenos resultados hacia modelos menos intensivos que requieren acudir menos veces a los establecimientos de salud. Los modelos diferenciados de prestación de servicios de TB pueden modificarse, con el fin de dar cabida a las diferentes necesidades de las personas con infección por el VIH de distintas edades. También pueden extenderse a los grupos poblacionales sin infección por el VIH con mayor riesgo de contraer la TB, incluidos los contactos del hogar de los pacientes con TB
Recientemente, se han puesto a prueba diferentes modelos diferenciados de prestación de TAR, entre ellos modelos de grupos dirigidos por trabajadores de salud, modelos impulsados por las personas que reciben el TPT, modelos individuales de prestación en un establecimiento y modelos individuales comunitarios. A continuación se brindan algunos ejemplos de los modelos diferenciados de prestación de servicios que se han implementado (75,76).
- Espaciamiento de las citas (modelo individual de prestación en un establecimiento): recetas para varios meses e instauración de un circuito rápido en los establecimientos de gran volumen de atención, con el fin de permitir que los pacientes estables reciban una evaluación rápida y procedan directamente a la farmacia para recoger los medicamentos.
- Puntos comunitarios de distribución de TAR (modelos individuales comunitarios): trabajadores sanitarios no profesionales realizan la evaluación y la distribución de medicamentos.
- Clubes de adhesión (en establecimientos y comunitarios): distribución del tratamiento durante las reuniones del grupo de apoyo (cada tres a seis meses).
- Consultorios especializados adaptados a los niños que proporcionan de dos a ocho semanas de suministro de TPT y TAR, según el plan de desplazamientos de cada beneficiario.
- Recogidas a distancia en farmacias comerciales o pastilleros (“distribuidores automáticos de medicamentos”) sin ninguna participación de trabajadores comunitarios de salud.
- Se prevé que las estrategias diferenciadas de prestación de servicios dirigida a las personas con infección por el VIH que están estables reducirán el abarrotamiento en los consultorios de TAR, favorecerán la calidad de la atención, mejorarán la adhesión y aumentarán las tasas de supresión viral, con mayor comodidad para las personas. Se prevé que estas estrategias permitan brindar apoyo y educación apropiados acerca de los posibles eventos adversos, la tolerabilidad y la importancia de finalizar el tratamiento. En principio, todos los servicios recomendados para la TB deben incorporarse en estos modelos de prestación de servicios y se deben aprovechar los mecanismos existentes de evaluación de la calidad de los servicios de TAR para supervisar la ejecución de los servicios de búsqueda intensificada de casos de TB y de TPT. En todos los programas diferenciados de prestación de servicios se deben considerar las siguientes intervenciones para la atención de la TB.
- Todos los servicios de TB y VIH recomendados que se ofrecen a las personas con infección por el VIH, incluidas las pruebas habituales de tamizaje de la TB, la derivación para diagnóstico cuando se observan síntomas de TB y el TPT cuando se descarta la enfermedad por TB, deben prestarse a intervalos regulares (al menos una vez por trimestre).
- El TPT puede iniciarse durante la evaluación previa al TAR o antes de comenzar las citas espaciadas en el marco de la prestación diferenciada de servicios, en especial con los esquemas acortados (1HP) o en el momento de la visita de seguimiento al centro de salud si se aplican los esquemas más largos (6H, 4R, 3HR, 3HP), en conformidad con las directrices nacionales.
Si bien es posible suministrar esquemas de TPT de cualquier duración en el marco de la prestación diferenciada de servicios, es fundamental establecer un mecanismo para detectar y manejar cualquier evento adverso, teniendo en cuenta la duración de los esquemas de TPT y documentar de manera sistemática los indicadores del TPT (véase el capítulo 8). En la figura 5.1 se muestran los elementos primordiales para integrar el TPT en las iniciativas de prestación diferenciada de servicios.
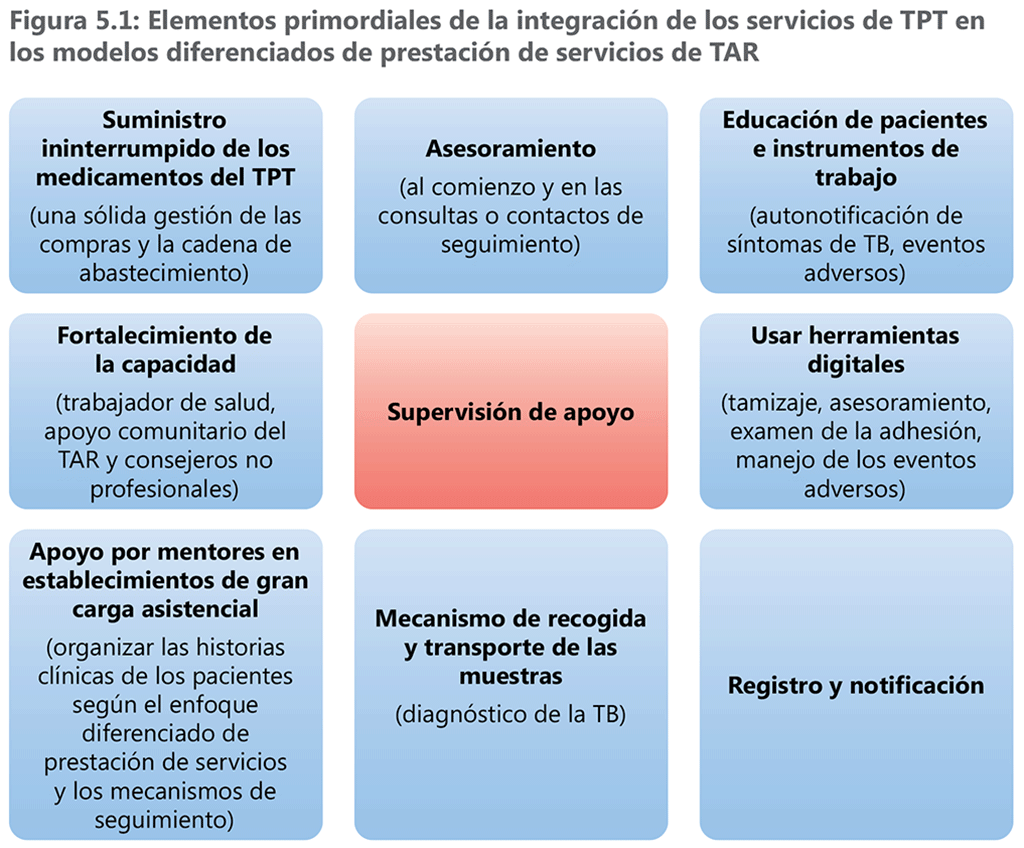
A medida que más países implementan la prestación diferenciada de servicios, se presenta una oportunidad clave de ampliar los servicios de TPT cuando el país decide hacer la transición al TAR a base de dolutegravir (u otros esquemas nuevos). Varios países en África oriental y meridional han decidido hacer coincidir la transición al esquema TLD (tenofovir, lamivudina, dolutegravir) con la ampliación de esquemas acortados de TPT (3HP). Dado que la transición a un nuevo TAR entraña un seguimiento clínico más frecuente, los programas nacionales también están aprovechando esta oportunidad para iniciar el TPT y generar experiencia en la ejecución para orientar la ampliación a escala nacional.
Punto clave: La prestación diferenciada de servicios del VIH se está ampliando en los servicios de ARV. La búsqueda intensificada de casos de TB y el TPT deben integrarse en estos modelos. La introducción de la prestación diferenciada de servicios no debe convertirse en una razón para retrasar o negar los beneficios del TPT a las personas con infección por el VIH. De hecho, las citas de los pacientes deben programarse de tal manera que puedan recoger al mismo tiempo los medicamentos ARV y el TPT.
Provisión de TPT a grupos especiales de la población
TPT en las mujeres durante el embarazo y el posparto
Las embarazadas con infección por el VIH corren un riesgo mayor de contraer la TB durante el embarazo y el posparto, lo que puede tener consecuencias graves para tanto la madre como para el lactante (77,78). El embarazo no debe descalificar a las embarazadas con infección por el VIH o seronegativas que reúnen los criterios para recibir el TPT, ya que la isoniacida y la rifampicina, que son los fármacos utilizados comúnmente en el tratamiento preventivo, se consideran seguros para su uso durante el embarazo (clasificados como categoría C en el embarazo por la Administración de Alimentos y Medicamentos de Estados Unidos) (79,80). La OMS realizó una revisión sistemática para la actualización del 2019 de las directrices sobre la ILTB, con el fin de evaluar la evidencia en favor o en contra del informe reciente de un ECA que mostraba un mayor riesgo de resultados adversos del embarazo con el TPI (81). Sin embargo, el examen de toda la demás evidencia existente no reprodujo ninguna asociación del TPI con resultados adversos del embarazo, como la muerte fetal o del neonato, la prematuridad, el peso bajo al nacer o las anomalías congénitas. Del mismo modo, no se comunicó ningún riesgo estadísticamente significativo de hepatotoxicidad materna, eventos de grado 3 o 4 ni de muerte. Por consiguiente, posiblemente no sea necesario aplazar el TPT al posparto y debería iniciarse el tratamiento preventivo durante el período prenatal y posnatal junto con la atención debida. Las pruebas de función hepática no están indicadas de manera sistemática cuando se administra el TPT durante el embarazo, a menos que existan otros peligros. El suplemento con vitamina B6 debe administrarse de ordinario a todas las embarazadas y las mujeres que amamantan y reciben TPT. En general, se considera que el uso de rifampicina es seguro durante el embarazo y no es necesario ajustar la posología, aunque no hay datos de seguridad o eficacia disponibles específicamente durante el embarazo y el posparto (82). Existen datos limitados sobre la eficacia y la seguridad de la rifapentina durante el embarazo y por lo tanto, no se deben usar los esquemas 1HP y 3HP en el embarazo hasta que se cuente con más datos de seguridad.8 Hasta que se disponga de estos datos, pueden utilizarse los comprimidos de combinación triple de isoniacida + B6 + cotrimoxazol en el TPT de las mujeres con infección por el VIH durante el embarazo y el posparto, con el debido apoyo y supervisión.
El tratamiento preventivo con isoniacida, rifampicina o ambas se puede administrar con seguridad a las mujeres que amamantan (83). Se debe aportar un suplemento de piridoxina (vitamina B6) al lactante que esté tomando isoniacida o cuando la mujer que lo amamanta esté tomando isoniacida. Al igual que en el caso de las embarazadas con infección por el VIH, los comprimidos de combinación triple de isoniacida + B6 + cotrimoxazol pueden usarse en las mujeres con la infección por el VIH que amamantan.
Punto clave: El comprimido de combinación triple de isoniacida + B6 + cotrimoxazol puede ser la opción preferida de TPT en las mujeres con infección por el VIH durante el embarazo y el posparto, hasta que se disponga de más datos de seguridad sobre el uso de esquemas acortados a base de rifapentina.
Mujeres que reciben anticonceptivos orales u hormonales
La rifampicina y la rifapentina interactúan con los medicamentos anticonceptivos orales y hormonales con un posible riesgo de disminución de la eficacia anticonceptiva. Las mujeres que reciben anticonceptivos orales mientras están tomando rifampicina o rifapentina deben ya sea:
- cambiar el anticonceptivo oral y usar otra opción (como el acetato de medroxiprogesterona de liberación prolongada cada ocho semanas (84) o una dosis más alta de estrógeno [50μ]) en consulta con un médico; o
- usar otro método de anticoncepción como un anticonceptivo de barrera o un dispositivo intrauterino
En las mujeres que tengan implantes hormonales anticonceptivos, puede ser necesario acortar de 12 a 8 semanas el intervalo para reemplazar los implantes (estudio ACTG A5338).
Hepatopatía o antecedentes de hepatopatía
La isoniacida y la rifampicina o la rifapentina se asocian con daño hepático. El TPT debe iniciarse con cuidado en las personas que cuenten con valores de base de la transaminasa hepática y en las que se haya determinado que dichos valores correspondían a más de tres veces el límite superior normal. No debe administrarse el tratamiento preventivo a las personas con hepatopatía terminal. Sin embargo, se sabe que las personas con infecciones crónicas por el virus de la hepatitis B o la hepatitis C toleran bien el TPT (85,86).
Hepatitis aguda (y hepatitis viral aguda)
Diferir el tratamiento preventivo hasta que se haya resuelto la hepatitis aguda.
Insuficiencia renal
La isoniacida y la rifampicina o la rifapentina se eliminan por excreción biliar. Por lo tanto, estos medicamentos pueden administrarse en las posologías habituales a los pacientes con insuficiencia renal. Los pacientes con insuficiencia renal grave deben recibir isoniacida con piridoxina (vitamina B6) a fin de prevenir la neuropatía periférica
Personas con infección por el VIH
Una dificultad considerable del TPT con el esquema a base de rifamicina en las personas con infección por el VIH es la interacción medicamentosa. No se requiere ajustar la dosis cuando la rifampicina y la rifapentina se administran de manera concomitante con efavirenz. Es necesario aumentar la posología de dolutegravir a 50 mg dos veces diarias cuando se administra con rifampicina (no se precisan ajustes de la dosis cuando se utiliza rifapentina). Los esquemas de TPT con rifampicina o rifapentina no se deben administrar conjuntamente con inhibidores de la proteasa o nevirapina (para más detalles véase la sección sobre interacciones medicamentosas)
Tratamiento de los recién nacidos de madres con TB activa
- Evalúe al recién nacido. Si el recién nacido no se encuentra bien, remítalo a un especialista o pediatra. Es importante garantizar que la madre reciba un tratamiento eficaz contra la TB para que deje de ser contagiosa. Además, asegúrese de que se apliquen las medidas de control de infecciones en la sala de neonatos, sobre todo si el bebé está en un centro de hospitalización por ser prematuro o pequeño al nacer.
- Si el recién nacido está bien (ausencia todo signo o síntoma indicativo de TB), administre el TPT y retrase la vacunación contra la TB (BCG), hasta que haya completado el TPT. Administre piridoxina en 5 a 10 mg diarios.
- Si el bebé se ha expuesto al VIH (madre con la infección por el VIH) y recibe nevirapina, debería iniciarse el TPI. El esquema de TPT con RH y HP no puede administrase junto con la profilaxis con nevirapina ya que las rifamicinas disminuyen la concentración de nevirapina y pueden aumentar la transmisión del VIH de la madre al hijo (87).
- Al final del TPT, realice la PT o el IGRA. Si el resultado es negativo para la infección por TB o la prueba no está disponible, administre la vacuna contra la TB (a menos que el bebé sea positivo al VIH).
- Si la madre está tomando medicamentos contra la TB, puede seguir amamantando sin riesgo. La madre y el bebé deben permanecer juntos, y la lactancia materna puede continuarse durante el TPT.
- Los bebés amamantados por una mujer que recibe un tratamiento contra la TB o el TPT deben recibir piridoxina mientras dure el tratamiento de la madre.
Contactos de pacientes con TB-MDR
Los contactos del hogar de los pacientes con TB-MDR o con monorresistencia a la isoniacida corren un riesgo mayor de contraer la infección por TB que los contactos expuestos a la TB farmacosensible; sin embargo, el riesgo de progresión hacia la enfermedad por TB no difiere entre los contactos de ambos grupos (88). Algunos estudios han comunicado una disminución cercana al 90% de la incidencia de TB-MDR con el TPT (89). La OMS recomienda el TPT en los contactos expuestos a pacientes con TB-MDR, tras considerar la intensidad de la exposición; confirmar el caso original y su tipo de farmacorresistencia (es decir, TB-MDR confirmada bacteriológicamente y sensibilidad establecida a una fluoroquinolona); y evaluar la presencia de infección por TB mediante el IGRA o la PT. Se busca así evitar los eventos adversos posibles con el uso de fluoroquinolona durante seis meses y preservar la opción de utilizar la fluoroquinolona en caso de que se aparezca una TB-MDR en los contactos
La OMS propone el uso de levofloxacina durante seis meses (presentación pediátrica para niños que son contactos) (véase la posología en el cuadro 5.2) junto con otros fármacos contra la TB como el etambutol o la etionamida, si se toleran. Independientemente de que administre o no el tratamiento, debe darse seguimiento clínico durante dos años, investigar activamente todo signo o síntoma indicativo de TB que aparezca y comenzar esquemas curativos cuando sea necesario. Los contactos de personas con TB resistente a la rifampicina se pueden tratar igual que los contactos de TB-MDR, pero cuando se confirma la sensibilidad a la isoniacida en el caso inicial, los contactos pueden recibir 6H o 9H. La evidencia es escasa sobre el esquema preferido de TPT en los contactos expuestos a personas con TB resistente a la isoniacida. Sin embargo, los datos del Perú indican que el TPI sigue siendo eficaz (88). Además, 4R puede ser otra opción de TPT en estas situaciones
Se necesitan con urgencia ensayos aleatorizados sobre el tratamiento preventivo de la TB-MDR para mejorar la base de la evidencia. Se espera que en los próximos años se cuente con los resultados de los siguientes tres ECA sobre el TPT en los contactos del hogar de pacientes con TB-MDR:
- TB CHAMP: evalúa seis meses de levofloxacina (Lfx) contra placebo en los lactantes y los menores de 5 años expuestos a la TB-MDR (Sudáfrica; inclusión en curso, con intención de publicarlo a finales del 2021; http://www.isrctn.com/ISRCTN92634082).
- V-QUIN: evalúa 24 semanas de Lfx contra placebo en todas las edades con pruebas de infección (Viet Nam; inclusión terminada; fecha de finalización de la recogida de datos marzo del 2022; https://anzctr.org.au/Trial/Registration/TrialReview.aspx?id=369817).
- PHOENIx: evalúa 26 semanas de delamanid contra isoniacida en todas las edades (11 países; se estima su finalización hacia mediados del 2025; https://clinicaltrials.gov/ct2/show/NCT03568383).
TPT y tratamiento contra el virus de la hepatitis C
No se recomienda el uso de rifamicinas, incluida la rifapentina, junto con muchos de los medicamentos ARV de acción directa que se utilizan en el tratamiento de la hepatitis C, ya que las rifamicinas pueden disminuir a niveles subterapéuticos la concentración de los fármacos contra el virus de la hepatitis C (90,91). Las personas con hepatitis C deben consultar con sus prestadores de atención de salud y comenzar un TPT a base de rifamicina, ya sea antes o después de finalizar el tratamiento de la hepatitis C.
TPT en personas que consumen drogas
Las personas que consumen drogas tienen una prevalencia más alta de la infección por TB y una incidencia más alta de la TB activa (92). La rifapentina no se ha estudiado de manera sistemática en estas personas. Sin embargo, se sabe que la rifampicina reduce la exposición a los tratamientos de sustitución de opioides como la metadona y la buprenorfina (93). En algunas personas, esto da lugar a un síndrome de abstinencia opiácea. Por esta razón, es necesario observar de cerca a las personas que toman esquemas de 3HP, 3HR o 4R al mismo tiempo que un tratamiento de sustitución de opioides, para detectar los signos de abstinencia opiácea y otros eventos adversos. Aumentar la dosis de metadona o buprenorfina cuando se toman rifamicinas puede disminuir el riesgo de abstinencia. El uso del TPI es seguro en las personas que consumen drogas, aunque es importante una vigilancia cuidadosa de la toxicidad hepática (94). El consumo de drogas nunca debe tomarse como una justificación general para negarle a alguien el TPT. Es responsabilidad de los prestadores de atención de salud de anticipar un manejo preventivo seguro de las interacciones medicamentosas en las personas que consumen drogas (95).
⁴ Véase el texto y el cuadro 5.2 sobre las opciones de TPT en casos de TB multirresistente (TB-MDR)
⁵ Precios de los catálogos de precios de referencia de GDF de la Alianza Alto a la Tuberculosis y del Fondo Mundial; Stichting Iplussolutions, proveedores para la garantía de calidad del Fondo Mundial Global, IDA Foundation y la Alianza para la gestión de la cadena de abastecimiento. http://www.stoptb.org/assets/documents/gdf/20191015%20GDF%20TB%20Medicines%20Budgeting%20Prices.pdf.
⁶ Datos del ensayo clínico NCT02651259, que evalúa la farmacocinética, la tolerabilidad y la seguridad de la rifapentina y la isoniacida una vez por semana durante el embarazo y el puerperio, en mujeres con infección latente por TB, con o sin infección por el VIH 1; se presentará en la Conferencia sobre retrovirus e infecciones oportunistas del 2020.
⁷ La isoniacida es metabolizada por la N-acetiltransferasa 2 (NAT2) y una mutación que modifica el genotipo de NAT2 da lugar a persistencia de la isoniacida en el organismo y mayor predisposición a la toxicidad. Se observan diferencias geográficas de la prevalencia de mutaciones de NAT2, ya que los acetiladores lentos (conocidos por su riesgo de presentar la mayor parte de toxicidades inducidas por los medicamentos) son muy comunes en algunos entornos (83% en Egipto y 67% en Estados Unidos), pero raros en otros (12% en China).
⁸ El estudio IMPAACT 2001, que se presentará en la Conferencia sobre Retrovirus e Infecciones Oportunistas del 2020, muestra la farmacocinética y la seguridad relativa de 3HP en las embarazadas, pero destaca la necesidad de más estudios.
 Reacción
Reacción