Enlaces transversales de Book para 4.1.1 Decision pathway for Algorithm 1 – mWRD as the initial diagnostic test for TB
El algoritmo 1 es el algoritmo de pruebas preferido para respaldar el diagnóstico de TB en las personas evaluadas por TB pulmonar y extrapulmonar. En este algoritmo, las PDRm se usan como la prueba diagnóstica inicial de la TB y la resistencia a la RIF (es decir, este algoritmo cumple las metas de la Estrategia Fin de la TB sobre el uso universal de PDRm y PSF). Este algoritmo está diseñado para ser utilizado con cada una de las PDRm aprobadas por la OMS en la detección del complejo M. tuberculosis (Xpert MTB/RIF, Xpert MTBRIF Ultra, Truenat MTB, Truenat MTB Plus y TB-LAMP), aunque puede precisar modificaciones menores según la PDRm utilizada y la población destinataria. Por ejemplo, si bien este algoritmo es apropiado en los entornos con carga alta o baja de TB MDR, en un entorno con una carga alta sería preferible usar una PDRm que detecte el complejo M. tuberculosis y la resistencia a la RIF de manera simultánea (por ejemplo, Xpert MTB/RIF), en lugar de una prueba que detecte solo el complejo M. tuberculosis (como el TB-LAMP).
La aplicación de este algoritmo es factible cuando la PDRm recomendada por la OMS se puede realizar en el mismo centro o se cuenta con acceso a un sistema fiable de derivación con lapsos cortos de obtención de resultados.
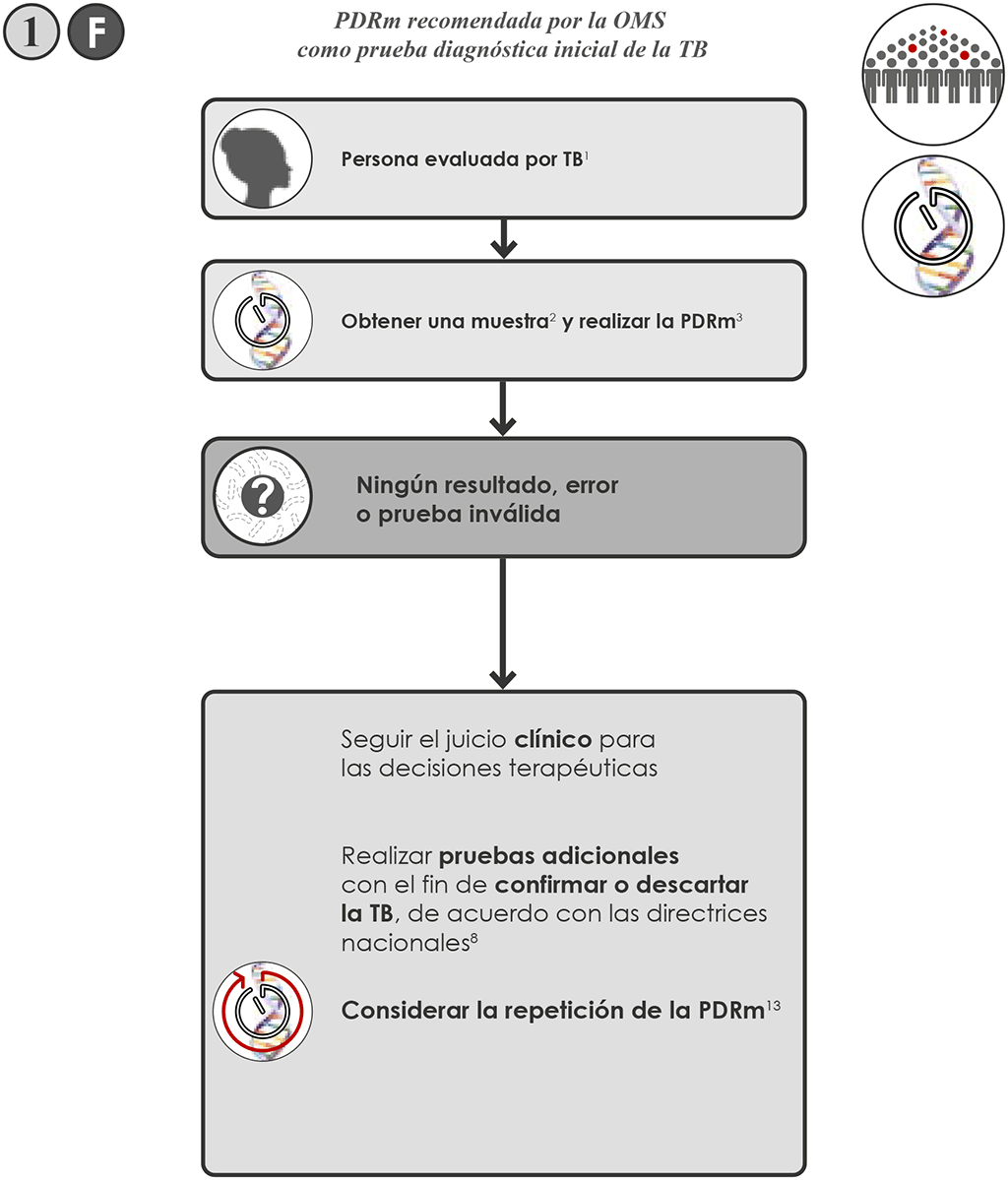
PDRm recomendada por la OMS como prueba diagnóstica inicial de la TB
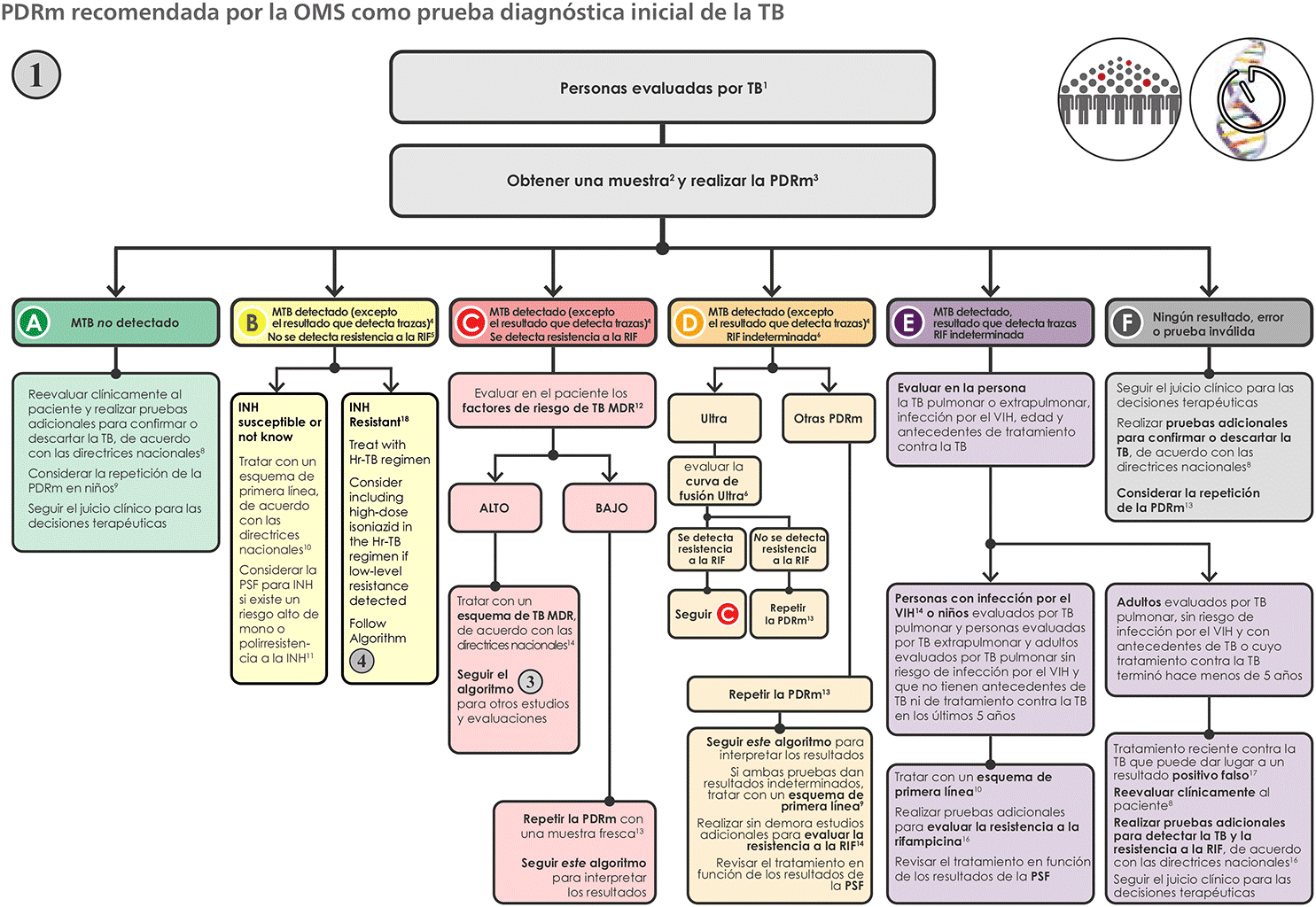
H: isoniacida; MTB: Mycobacterium tuberculosis; PDRm: prueba molecular de diagnóstico rápido (recomendada por la OMS); PSF: prueba de sensibilidad a los fármacos; RIF: rifampicina; TB: tuberculosis; TB MDR: tuberculosis multirresistente; TB RR: tuberculosis resistente a la rifampicina; VIH: virus de la inmunodeficiencia humana.
1 En las personas evaluadas por TB se incluyen adultos y niños con signos o síntomas indicativos de TB o con imágenes anormales en la radiografía de tórax indicativas de TB. También se puede seguir este algoritmo en el diagnóstico de la TB extrapulmonar usando muestras de LCR, ganglios linfáticos y otros tejidos.
2 Los programas pueden considerar la posibilidad de obtener dos muestras de entrada. La primera muestra se debe examinar de inmediato con una PDRm recomendada por la OMS. La segunda muestra se puede usar para las pruebas adicionales descritas en este algoritmo. En las personas evaluadas por TB pulmonar, el esputo es la muestra preferida. Las biopsias de tejidos son difíciles o imposibles de obtener de manera reiteraa; por consiguiente, se deben examinar con tantos métodos como sea posible (por ejemplo, PDRm, cultivo, PSF o examen histológico). 3 Las PDRm recomendadas por la OMS apropiadas en este algoritmo son Xpert MTB/RIF, Xpert Ultra, Truenat MTB, Truenat MTB Plus y TB LAMP.
6 MTB detectado (excepto el resultado que detecta trazas)” incluye MTB detectado alto, moderado, bajo o muy bajo. Estas categorías se aplican a las pruebas originales Xpert MTB/RIF e Xpert Ultra. Los resultados de Truenat MTB y MTB Plus y TB-LAMP también entran en esta categoría de “MTB detectado ( excepto el resultado que detecta trazas)”.
5 La determinación de resistencia a la RIF es simultánea en la prueba Xpert MTB/RIF e Xpert Ultra. Se necesita una segunda prueba para determinar la resistencia a la RIF cuando se realizaron las pruebas Truenat MTB y MTB Plus, usando el mismo ADN que se aisló para las pruebas Truenat MTB (prueba Truenat MTB RIF Dx, véase la figura 3.1) o cuando se realizó TB LAMP, en cuyo caso se necesita la obtención de una muestra fresca y la realización de PSF molecular o fenotípica.
6 La interpretación y las pruebas de seguimiento de los resultados “MTB detectado, rifampicina indeterminada” de la prueba Xpert Ultra son diferentes de la interpretación de los resultados de otras PDRm. Los resultados MTB detectado, rifampicina indeterminada de Xpert Ultra (sobre todo con resultados semicuantitativos altos y medios) pueden deberse a deleciones grandes o mutaciones múltiples que confieren resistencia a la RIF. El análisis de las curvas de fusión Ultra puede detectar estas mutaciones que confieren resistencia. En algunos casos, se necesitará el cultivo y la PSF, la secuenciación o la LPA PL con el fin de confirmar o excluir la resistencia a la RIF. Los resultados indeterminados de las demás PDRm se relacionan a menudo con cantidades muy escasas de bacilos en la muestra.
7 “MTB detectado, trazas” se aplica solo a la prueba Xpert Ultra.
8 Otras investigaciones para detectar la TB pueden incluir la radiografía de tórax, valoraciones clínicas adicionales, la repetición de la PDRm, el cultivo o la respuesta clínica tras un tratamiento con antimicrobianos de amplio espectro.
9 En niños con signos y síntomas de TB pulmonar en los entornos con una probabilidad previa a la prueba de 5% o más y un resultado negativo de Xpert MTB/RIF o Xpert Ultra en la prueba inicial, se repite la prueba Xpert MTB/RIF en esputo o aspirado nasofaríngeo (un total de dos pruebas). Además, la prueba Xpert MTB/RIF puede usarse en líquido gástrico y heces. No hubo datos disponibles para evaluar el rendimiento de la prueba Xpert Ultra en muestras de líquido gástrico y heces. Se estimula a los programas a utilizar la prueba Xpert Ultra en muestras de líquido gástrico y heces, en condiciones de investigación operativa. La PDRm debe repetirse en el mismo centro de pruebas con una muestra fresca y el resultado de la repetición se interpreta como se indica en este algoritmo. El resultado de la segunda prueba es el resultado que debe usarse en las decisiones clínicas.
10 Los pacientes deben iniciar un esquema de primera línea según las directrices nacionales, a menos que el paciente tenga riesgo muy alto de tener TB MDR. En estos pacientes se debe iniciar un esquema de TB MDR.
11 Se puede enviar una muestra para PSF molecular o fenotípica de INH si en este entorno existe una prevalencia alta de resistencia a la INH, no asociada con resistencia a la RIF (es decir, mono o polirresistencia a la INH).
12 Los pacientes con riesgo alto de TB MDR incluyen los pacientes tratados anteriormente, incluidos los perdidos durante el seguimiento, las recaídas o los fracasos terapéuticos; la falta de conversión (con baciloscopia positiva a final de la fase intensiva); los contactos de casos de TB MDR; y otros grupos de riesgo de TB MDR reconocidos en el país.
13 La PDRm se debe repetir en el mismo centro de pruebas con una muestra fresca y el resultado de la repetición se interpreta como se indica en este algoritmo. El resultado de la segunda prueba es el resultado que debe usarse en las decisiones clínicas.
14 En las personas con infección por el VIH se incluyen las personas positivas al VIH o cuya situación frente al VIH se desconoce, pero que se presentan con fuerte evidencia clínica de infección por el VIH en entornos donde hay una prevalencia alta de esta infección o en los miembros de grupos con alto riesgo de contraer el VIH. En todas las personas con estado desconocido frente al VIH, deben realizarse pruebas de detección del VIH según las directrices nacionales.
15 El paciente debe iniciar sin demora un esquema de TB MDR de acuerdo con las directrices nacionales. Se debe seguir el algoritmo 3 para las pruebas adicionales de todo paciente con TB RR.
16 Existen métodos disponibles fenotípicos (cultivo y PSF) y moleculares (por ejemplo, LPA, secuenciación de ADN y pruebas centralizadas con equipamiento de alto rendimiento) para evaluar la farmacorresistencia. Se prefieren los métodos moleculares rápidos.
17 En los pacientes con antecedentes de TB en los últimos 5 años o cuyo tratamiento de la TB se completó hace menos de 5 años, los resultados que detectan una traza en la prueba Xpert Ultra (y en ocasiones el resultado “detectado, bajo o muy bajo” de la prueba Xpert MTB/RIF)pueden ser positivos, no por causa de una TB activa sino por la presencia de bacilos no viables. No se recomienda repetir la prueba Xpert MTB/RIF ni la Xpert Ultra, pero pueden usarse como un intento inicial para evaluar la resistencia a la RIF. El cultivo y la PSF pueden ser útiles para detectar la TB y la farmacorresistencia. Las decisiones clínicas deben tomarse con toda la información disponible y según el juicio clínico.
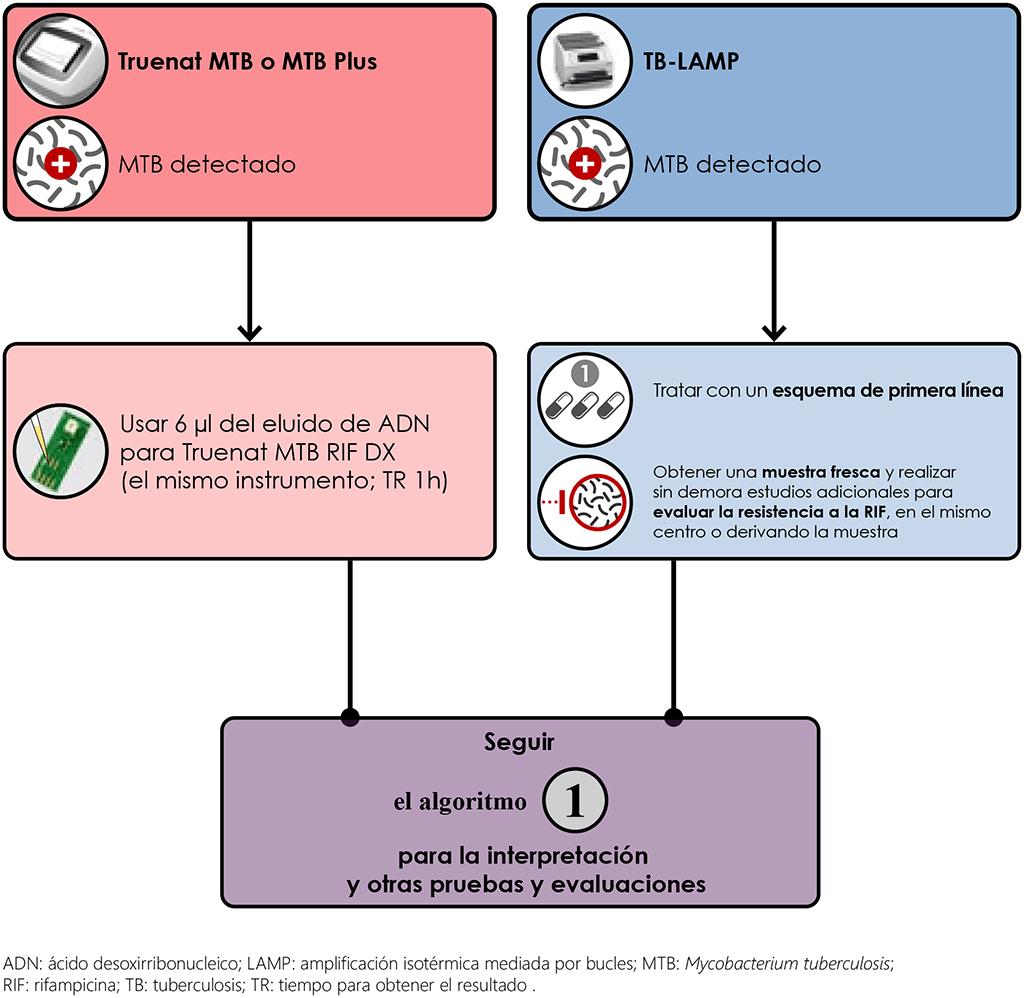
Figura 3.1 Prueba en dos etapas de la resistencia a la RIF con Truenat y TB LAMP
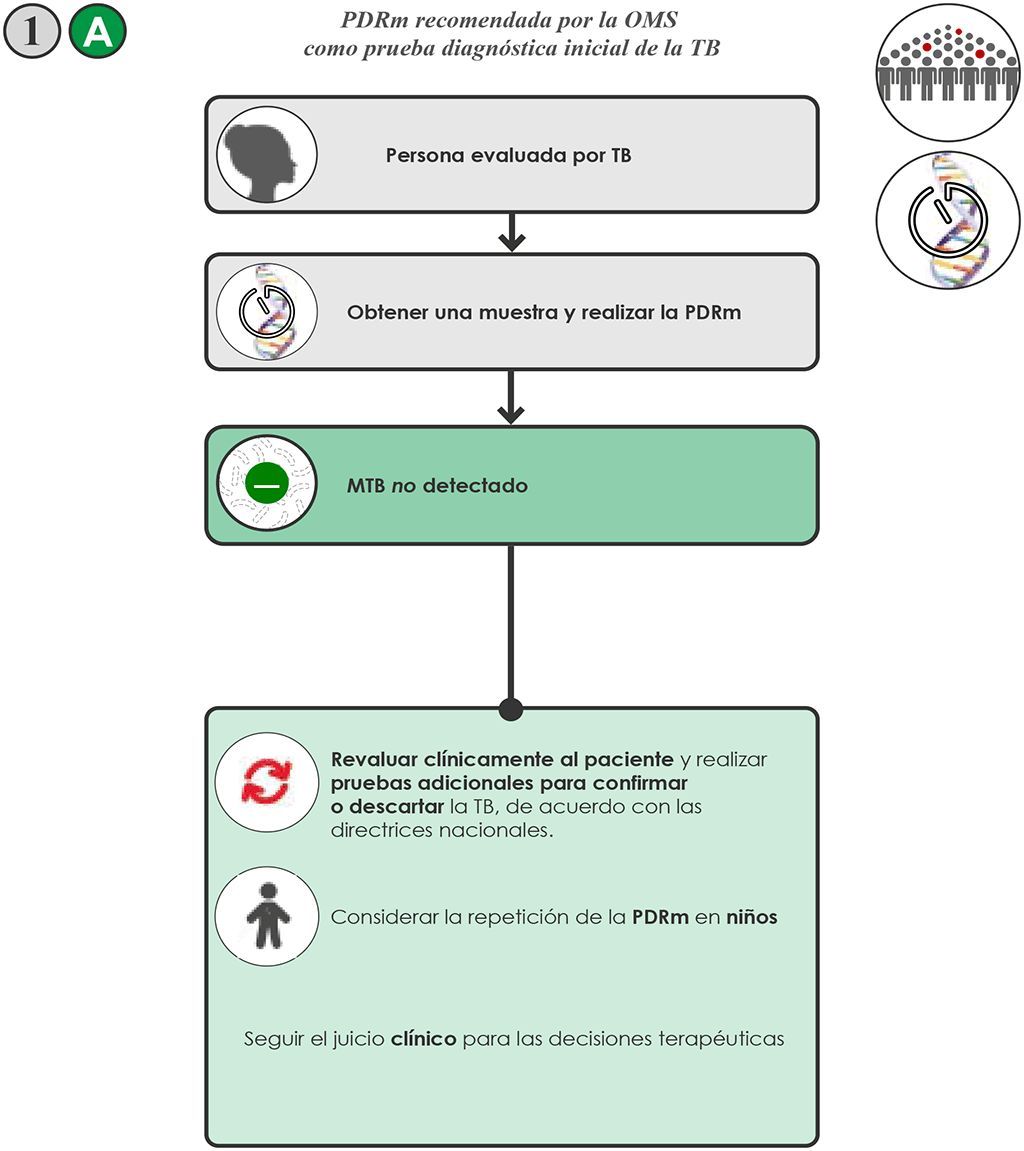
Ruta de las decisiones en el algoritmo 1: PDRm recomendada por la OMS como prueba diagnóstica inicial de la TB
Pruebas
Las PDRm adecuadas en este algoritmo incluyen la prueba Xpert MTB/RIF, Xpert MTB/RIF Ultra, Truenat MTB, Truenat MTB Plus y TB LAMP.
- La “prueba Xpert MTB” designa ya sea la prueba Xpert MTB/RIF original o la prueba Xpert MTB/RIF Ultra (en adelante denominada “Xpert Ultra”). Se nombran las pruebas individuales cuando se describen características específicas de cada una.
- Las pruebas Truenat® MTB y MTB Plus utilizan las mismas categorías de resultados que la prueba Xpert MTB/RIF y la ruta de las decisiones de las pruebas Truenat es la misma que la de Xpert MTB/RIF.
- Con respecto a la detección de resistencia a la RIF, las pruebas Xpert MTB detectan el MTB y la resistencia a la RIF de manera simultánea. En una muestra con un resultado positivo de Truenat MTB o MTB Plus se continua el estudio con Truenat MTB-RIF Dx, usando la misma muestra de ADN que se aisló para la prueba Truenat inicial. Una prueba TB-LAMP positiva exige la obtención de una muestra fresca y la realización de la PSF molecular o fenotípica para detectar la resistencia a la RIF.
Consideraciones generales
La OMS recomienda el uso de una PDRm (Xpert MTB/RIF, Xpert MTB/RIF Ultra, Truenat MTB, Truenat MTB Plus, Truenat MTB RIF Dx o TB-LAMP) como la prueba diagnóstica inicial, en reemplazo de la microscopia o el cultivo, en todas las personas con signos y síntomas de TB. Esto incluye a todas las personas sintomáticas que acuden por primera vez y también puede incluir a los pacientes que están en tratamiento o que recibieron tratamiento anteriormente, cuando el paciente se investiga por posible TB-RR (por ejemplo, en ausencia de conversión al final de la fase intensiva de tratamiento) o por un episodio de TB nuevo o persistente (por ejemplo, casos de recaída o pacientes tratados previamente, incluidos los perdidos durante el seguimiento). Los programas de TB deben operar la transición de la microscopia como prueba diagnóstica inicial hacia las PDRm que permiten la detección del complejo M. tuberculosis.
Este algoritmo se diseñó para ser usado con cada una de las PDRm para la detección del complejo M. tuberculosis, pero el algoritmo puede necesitar una modificación menor, según la PDRm que se utilice y en qué población.
- La prueba Xpert MTB/RIF e Xpert Ultra se recomiendan en los adultos y los niños evaluados por TB pulmonar; estas pruebas detectan el complejo M. tuberculosis y la resistencia a la RIF de manera simultánea.
- La prueba Xpert MTB también se recomienda para ser usada con muestras de LCR (muestra preferida en caso de meningitis tuberculosa) y con aspirados o biopsias de ganglios linfáticos. Además, la prueba Xpert MTB/RIF se recomienda con muestras de líquido pleural, líquido peritoneal, líquido pericárdico, líquido sinovial u orina, como la prueba diagnóstica inicial de la TB extrapulmonar correspondiente. Asimismo, se puede usar una muestra de sangre en adultos y niños positivos al VIH con signos y síntomas de TB diseminada.
- Las modificaciones menores necesarias al utilizar la prueba Xpert MTB en niños con signos y síntomas de TB pulmonar incluyen las siguientes:
- Xpert MTB/RIF puede usarse como la prueba diagnóstica inicial de la TB pulmonar en muestras de esputo, aspirado gástrico, aspirado nasofaríngeo o heces, y la prueba Xpert Ultra se recomienda en muestras de esputo y aspirado nasofaríngeo; y
- en los entornos con una probabilidad previa a la prueba de 5% o más y un resultado negativo de la prueba Xpert MTB como prueba inicial, se puede repetir la Xpert MTB con el mismo tipo de muestra u otros tipos (un total de dos pruebas); en otros casos, no se recomienda repetir la prueba.
- Las pruebas Truenat MTB y MTB Plus se recomiendan en la investigación de adultos y niños con signos y síntomas de TB pulmonar. Estas pruebas solo detectan el complejo M. tuberculosis. Se realiza una segunda prueba (Truenat MTB-RIF Dx) con el ADN aislado para la prueba Truenat MTB o MTB Plus con el fin de evaluar la resistencia a la RIF (esta prueba usa el mismo instrumento y el resultado tarda cerca de una hora; véase la figura 3.1). Con estas pruebas se deben tener en cuenta los siguientes aspectos:
- Hay incertidumbre acerca de la utilización de esta prueba en las personas con infección por el VIH, porque los datos disponibles sobre la realización de estas pruebas en este grupo son insuficientes. Se usaron datos indirectos sobre el rendimiento de estas pruebas en los pacientes con baciloscopia negativa para extrapolar la recomendación de uso en las personas con la infección por el VIH.
- En el caso de la población infantil, los datos disponibles solo fueron suficientes para recomendar la utilización de estas pruebas en las muestras de esputo. No había datos sobre el rendimiento de las pruebas con otras muestras.
- Se desconoce el rendimiento de esta prueba en la detección de la TB extrapulmonar
- La prueba TB-LAMP se recomienda como prueba de reemplazo de la baciloscopia de esputo y su uso sería apropiado en los entornos con una prevalencia baja de infección por el VIH y TB MDR. Con esta prueba se deben tener en cuenta los siguientes aspectos:
- En la población con carga alta de TB-MDR, TB-LAMP no debe reemplazar la utilización de pruebas moleculares rápidas que detectan la resistencia a la RIF (por ejemplo, Xpert MTB/RIF), porque TB-LAMP no suministra ninguna información sobre la resistencia a la RIF.
- En la población con prevalencia alta de infección por el VIH, TB-LAMP no debe reemplazar la utilización de las pruebas moleculares rápidas que tienen una sensibilidad más alta en la detección de la TB (por ejemplo, Xpert Ultra).
La prueba Xpert Ultra tiene dos diferencias notables en comparación con otras PDRm que se incorporaron en el algoritmo 1: primero, Xpert Ultra tiene un resultado semicuantitativo adicional de “MTB detectado, trazas”; y segundo, la evaluación de un resultado “MTB detectado, resistencia a la RIF indeterminada” difiere de la Xpert Ultra y otras PDRm. Estas diferencias se incorporaron en el algoritmo 1.
- La prueba Xpert Ultra tiene una sensibilidad mayor que las demás PDRm en la detección del complejo M. tuberculosis. Sin embargo, la sensibilidad más alta de Xpert Ultra se asocia con una ligera pérdida de especificidad (es decir, un aumento del número de pacientes calificados con un diagnóstico incorrecto de TB activa). Esto se debe a que la prueba Xpert Ultra detecta cantidades muy pequeñas de bacilos no viables o que no se multiplican, sobre todo en los pacientes con antecedentes de tratamiento de la TB (es decir, completado en los últimos 5 años). Otras PDRm pueden detectar estas bacterias no viables, aunque con menor frecuencia. Dado que la mayor sensibilidad y la pérdida de especificidad se asocian sobre todo con la indicación de “trazas” de Xpert Ultra, el algoritmo y la ruta de las decisiones incluyen criterios para la interpretación del resultado “MTB detectado, trazas”, con el fin de equilibrar los posibles daños del tratamiento excesivo de pacientes con un resultado positivo falso y los posibles beneficios de un aumento del número de pacientes con TB diagnosticada correctamente y la disminución de la mortalidad asociada con la TB.
- La prueba Xpert Ultra emplea un análisis basado en la temperatura de fusión (Tm) para detectar la resistencia a la RIF, en lugar de la PCR en tiempo real de las demás PDRm. Esta característica permite que la prueba Xpert Ultra diferencie mejor las mutaciones silenciosas de las mutaciones que confieren resistencia y mejora la precisión de la determinación de resistencia a la RIF. El programa informático de Xpert Ultra presenta un resultado de “RIF indeterminada” cuando una o varias de las sondas rpoB no producen ningún pico cuantificable de Tm (25). Esto puede suceder cuando existen deleciones grandes o mutaciones múltiples en la región que determina la resistencia a la RIF (RDRR). Con un análisis detallado de las curvas de fusión generadas por la prueba Xpert Ultra se reconocen estas mutaciones y por lo tanto se detecta la resistencia a la RIF sin las pruebas adicionales que se necesitan frente a un resultado RIF indeterminada de otras PDRm.
Las PDRm no se recomiendan como pruebas de seguimiento del tratamiento porque la presencia de bacilos muertos puede generar un resultado positivo. En su lugar, pueden utilizarse la microscopia y el cultivo, de acuerdo con las directrices nacionales y las recomendaciones de la OMS.
El algoritmo 1 describe la obtención de una muestra inicial para una PDRm recomendada por la OMS y la obtención de muestras adicionales, según sea necesario. Por cuestiones operativas, los programas pueden decidir obtener dos muestras (por ejemplo, una muestra inmediata en el momento de la consulta y una matinal de esputo o dos muestras inmediatas) de cada paciente de manera sistemática, en lugar de obtener la segunda muestra solo cuando se necesite una prueba adicional. En ese caso, la primera muestra debe analizarse sin demora mediante una PDRm. La segunda muestra puede usarse para la prueba adicional descrita en el algoritmo (por ejemplo, repetición de la PDRm) o la baciloscopia o el cultivo como línea de base para el seguimiento del tratamiento.
- Si no se puede obtener más de una muestra (por ejemplo, cuando las biopsias de tejido son difíciles o imposibles de obtener de manera reiterada), el algoritmo diagnóstico de la TB debería modificarse con el fin de dar prioridad a la PDRm. Cuando se justifica una prueba de TB adicional, una opción consiste en la posibilidad de utilizar para otras pruebas la fracción de la muestra que quedó después de realizar la PDRm (por ejemplo, cultivo, examen histológico, LPA y PSF). Las decisiones clínicas se deben tomar según el juicio clínico y los resultados disponibles de las pruebas de laboratorio.
Con respecto a la detección del complejo M. tuberculosis, los informes de las pruebas Xpert MTB/RIF, Xpert Ultra y Truenat MTB pueden ser “MTB no detectado”, “MTB detectado (alto, medio, bajo o muy bajo)”, “ningún resultado”, “error” o “inválida”. La prueba Xpert Ultra tiene otra categoría semicuantitativa “traza”. En la prueba TB-LAMP solo se informa “MTB detectado” o “MTB no detectado”.
- Cada una de las categorías semicuantitativas del MTB detectado, incluidos los resultados que detectan una traza, se considera como una confirmación bacteriológica de la TB.
- En los pacientes adultos sintomáticos, negativos al VIH, con antecedentes reciente de tratamiento contra la TB (es decir tratamiento completado hace menos de 5 años), los resultados que detectan una traza en la prueba Xpert Ultra (y en ocasiones de otras PDRm con “MTB detectado muy bajo”) pueden ser positivos no debido a una TB activa sino a la presencia de bacilos no viables. Las decisiones clínicas deben tomarse teniendo en cuenta toda la información disponible y el juicio clínico.
Con respecto a la detección de resistencia a la RIF, los informes de las pruebas Xpert MTB/ RIF, Xpert Ultra y Truenat MTB RIF Dx pueden ser “se detecta resistencia a la RIF”, “no se detecta resistencia a la RIF” o “indeterminada”. Estas pruebas infieren la resistencia a la RIF de la falta de unión de los amplicones a las secuencias de tipo salvaje. El uso del análisis de la temperatura de fusión, en lugar del análisis de la PCR en tiempo real en las pruebas Xpert Ultra y Truenat MTB/RIF mejora la fiabilidad de la detección de las mutaciones que confieren resistencia.
El uso de una PDRm con el fin de detectar la resistencia a la RIF no elimina la necesidad de la PSF clásica basada en el cultivo para determinar la resistencia a otros fármacos contra la TB y vigilar la aparición de otras farmacorresistencias.
- Obtener una muestra de buena calidad y transportarla al laboratorio que realiza la prueba. Realizar la PDRm recomendada por la OMS. En el caso de personas evaluadas por TB pulmonar, se pueden usar las siguientes muestras: esputo inducido o espontáneo (preferido), lavado broncoalveolar, lavado o aspirado gástrico, aspirado nasofaríngeo y heces (para información sobre el tipo de muestra que puede usarse con cada PDRm, véase arriba la sección 2.2 o las declaraciones de política específicas de la OMS).
- Si el resultado de la PDRm es “MTB no detectado” 1A, evaluar de nuevo al paciente y realizar pruebas adicionales según con las directrices nacionales.
- Otras investigaciones complementarias para detectar la TB pueden incluir la radiografía de tórax, valoraciones clínicas adicionales, PDRm adicionales o cultivos y, por último, la respuesta clínica a un tratamiento con antimicrobianos de amplio espectro (no deben usarse FQ).
- En niños con signos y síntomas de TB pulmonar en entornos con una probabilidad previa a la prueba superior a 5% (pero no en los entornos con una probabilidad previa al análisis inferior a 5%) y un resultado negativo de Xpert MTB en la primera prueba inicial, repetir la prueba Xpert MTB hasta un total de dos pruebas. Se pueden emplear los mismos tipos de muestra o tipos diferentes (por ejemplo, una muestra de esputo y una muestra de aspirado nasofaríngeo).
- Se desconoce el rendimiento de otras PDRm en la repetición de la prueba
- Considerar la posibilidad de una TB definida clínicamente (es decir, TB sin confirmación bacteriológica). Seguir el juicio clínico para las decisiones terapéuticas.
- Otras investigaciones complementarias para detectar la TB pueden incluir la radiografía de tórax, valoraciones clínicas adicionales, PDRm adicionales o cultivos y, por último, la respuesta clínica a un tratamiento con antimicrobianos de amplio espectro (no deben usarse FQ).
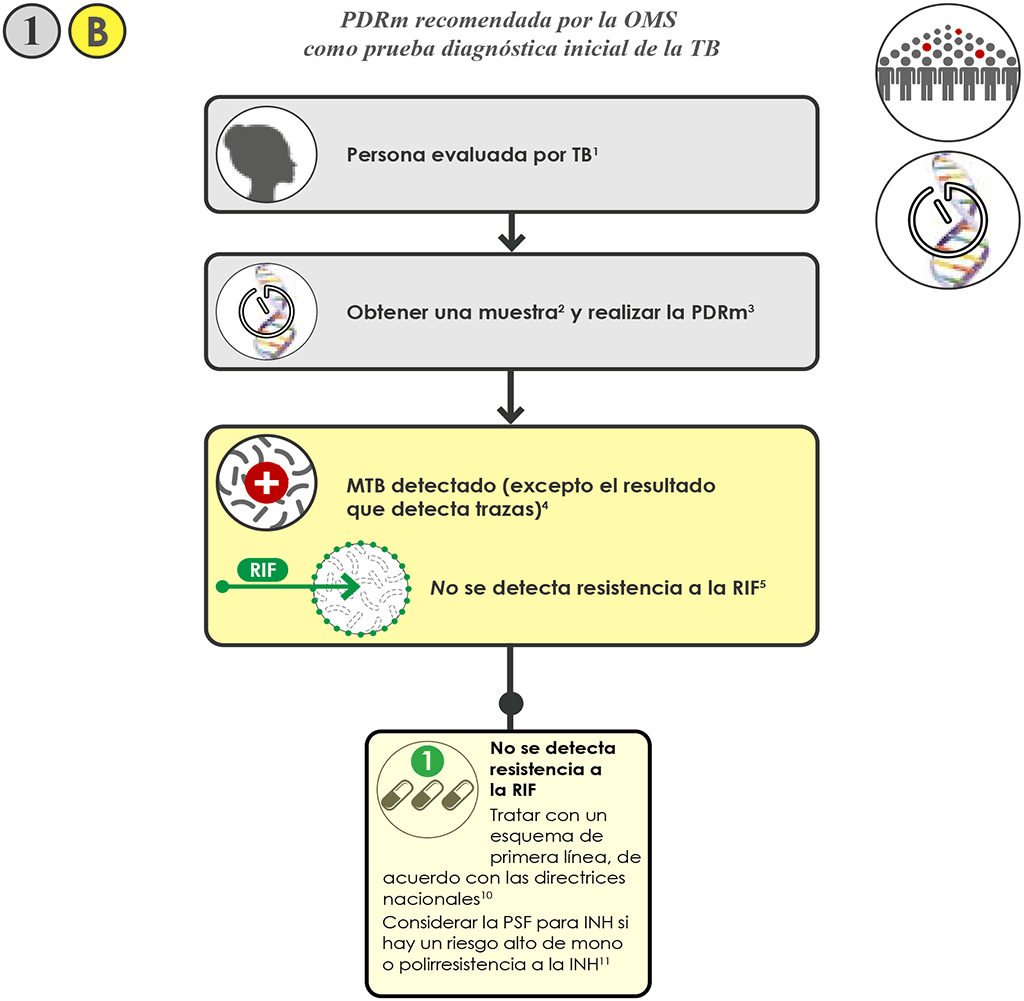
- Si el resultado de la PDRm es “MTB detectado, no se detecta resistencia a la RIF” 1 B :
- Iniciar en el paciente un esquema apropiado con fármacos contra la TB de primera línea, de acuerdo con las directrices nacionales.
- Solicitar PSF adicional en los siguientes casos:
- La PSF molecular o fenotípica para INH está indicada en especial:
- si el paciente ha recibido tratamiento con INH o es contacto de un paciente con TB rH conocido; o
- si en este entorno existe una prevalencia alta de resistencia a la INH que no está asociada con resistencia a la RIF (es decir, mono o polirresistencia a la INH, pero no TB MDR) (véase el algoritmo 4 para la prueba de seguimiento).
- La PSF molecular o fenotípica para RIF se puede solicitar si se considera que el paciente tiene riesgo de tener TB RR, a pesar del resultado de la PDRm inicial. Los resultados falsos de sensibilidad a la RIF con la prueba Xpert MTB son raros, pero se han observado en 1% a 5% de los casos de TB examinados en diversos entornos epidemiológicos. Por el contrario, la PSF fenotípica para RIF, sobre todo con cultivos en medio líquido, se asocia con una proporción mayor de resultados falsos de sensibilidad (26).
- La PSF molecular o fenotípica para INH está indicada en especial:
- En el caso de realizar pruebas adicionales moleculares o fenotípicas:
- Las pruebas moleculares y fenotípicas se pueden realizar en laboratorios diferentes. Realizar estas pruebas de manera simultánea, sin esperar los resultados de una prueba para iniciar la otra.
- Las PSF moleculares y fenotípicas se pueden realizar en la muestra (PSF directa) o en micobacterias recuperadas del cultivo (PSF indirecta). Para el análisis molecular se prefiere la PSF directa y se puede preferir la PSF indirecta con las pruebas fenotípicas, debido a aspectos técnicos relacionados con la producción de un inóculo apropiado y las pérdidas por contaminación.
- Se prefiere una prueba molecular rápida. En la actualidad, la LPA-PL es la única PDRm aprobada por la OMS para la resistencia a la INH. La LPA-PL detecta las mutaciones en inhA y katG, que orientan a los médicos en la composición del esquema para la TB resistente a la INH (véase el algoritmo 3). Se pueden consultar directrices sobre la interpretación de los resultados de la LPA en la guía correspondiente de la GLI (27). La secuenciación del ADN ha resultado útil en muchos casos, pero la OMS todavía no ha evaluado este método.
- La PSF fenotípica para INH y RIF basada en el cultivo requiere de 3 a 8 semanas para dar un resultado. La PSF fenotípica puede ser útil en la evaluación de los pacientes con un resultado negativo de la LPA-PL, sobre todo en los grupos poblacionales con una probabilidad alta previa a la prueba de resistencia a la INH.
- Si el resultado de la PDRm es “MTB detectado, se detecta resistencia a la RIF” 1 C, se necesita una evaluación del riesgo de TB-MDR. Los pacientes con un riesgo alto de TB-MDR son los pacientes anteriormente tratados como los perdidos durante el seguimiento, las recaídas o los fracasos terapéuticos; la falta de conversión (por ejemplo, con baciloscopia positiva a final de la fase intensiva del tratamiento de la TB sensible a los medicamentos); los contactos de pacientes con TB-MDR; y otros grupos de riesgo de TB-MDR reconocidos en el país. En los países con carga alta de TB-MDR, todo paciente con TB se considera con riesgo alto de tener TB-MDR.
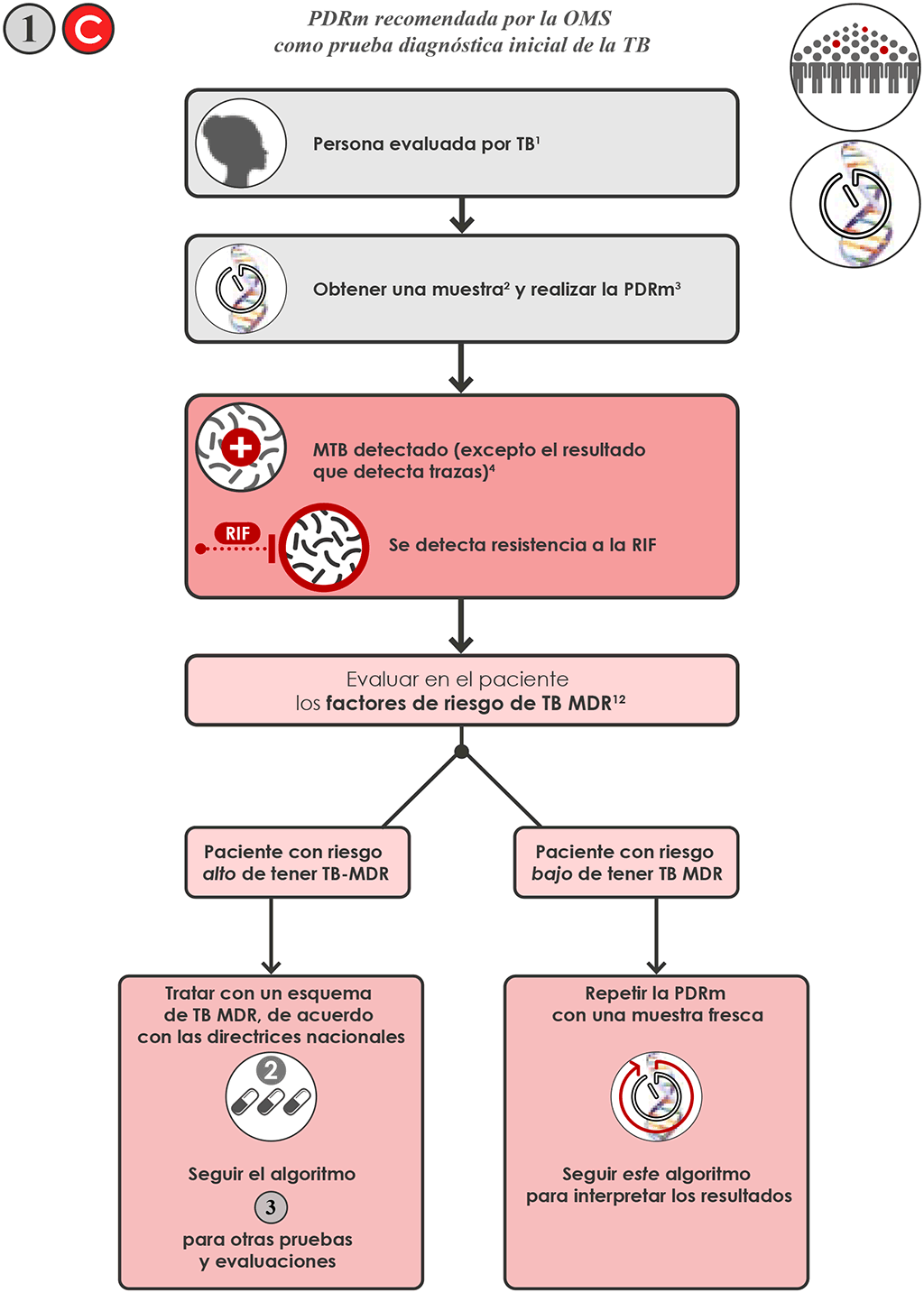
- Si el paciente tiene un riesgo alto de tener TB-MDR y el resultado de resistencia la RIF es definitivo, iniciar en el paciente un esquema de TB RR o TB MDR, de acuerdo con las directrices nacionales (3, 4). Seguir el algoritmo 3 para las pruebas adicionales.
- Si el paciente tiene un riesgo bajo de tener TB-MDR, repetir la PDRm con una segunda muestra. Si se cuenta con la LPA-PL en el centro y la muestra de esputo tuvo una baciloscopia positiva, se puede usar la LPA-PL para confirmar el resultado de resistencia a la RIF.
- Si la segunda prueba también indica resistencia a la RIF, iniciar un esquema de TB MDR de acuerdo con las directrices nacionales y las recomendaciones de la OMS (26, 27), y seguir el algoritmo 3 para las pruebas adicionales.
- Si el resultado de la PDRm en la segunda muestra es “MTB detectado, no se detecta resistencia a la RIF”, iniciar el tratamiento con un esquema de primera línea de acuerdo con las directrices nacionales. En la mayoría de las situaciones, los resultados falsos de resistencia a la RIF debidos problemas técnicos de la misma prueba son raros; sin embargo, pueden ocurrir debido a errores de laboratorio o de transcripción. Se supone que la repetición de la prueba se hará con más cuidado, que el resultado de la segunda prueba es correcto y que el resultado de la primera prueba pudo deberse a un error de laboratorio o de transcripción.
- . En todos los pacientes con TB-RR o TB-MDR, realizar estudios adicionales para evaluar la resistencia a los fármacos utilizados en el esquema de tratamiento. Se cuenta con métodos fenotípicos (cultivo y PSF) y moleculares (por ejemplo, LPA, secuenciación de ADN y pruebas con equipamiento de alto rendimiento) para evaluar la farmacorresistencia. Se prefieren los métodos moleculares rápidos.
- En el caso de los esquemas para la TB-MDR que utilizan FQ, enviar una muestra para análisis molecular de la resistencia a la FQ (véase el algoritmo 3).
- En condiciones ideales, se debería enviar una muestra de cada paciente para realizar PSF frente a cada uno de los fármacos utilizados en el esquema, para los cuales haya una prueba fiable. Sin embargo, no se debe retrasar el inicio del tratamiento por esperar los resultados de la PSF (el resultado de una PSF fenotípica puede tardar de semanas a meses).
- En todo cultivo positivo recuperado durante el seguimiento del tratamiento que sugiera un fracaso terapéutico se debe realizar una PSF a los fármacos que contenga el esquema de tratamiento.
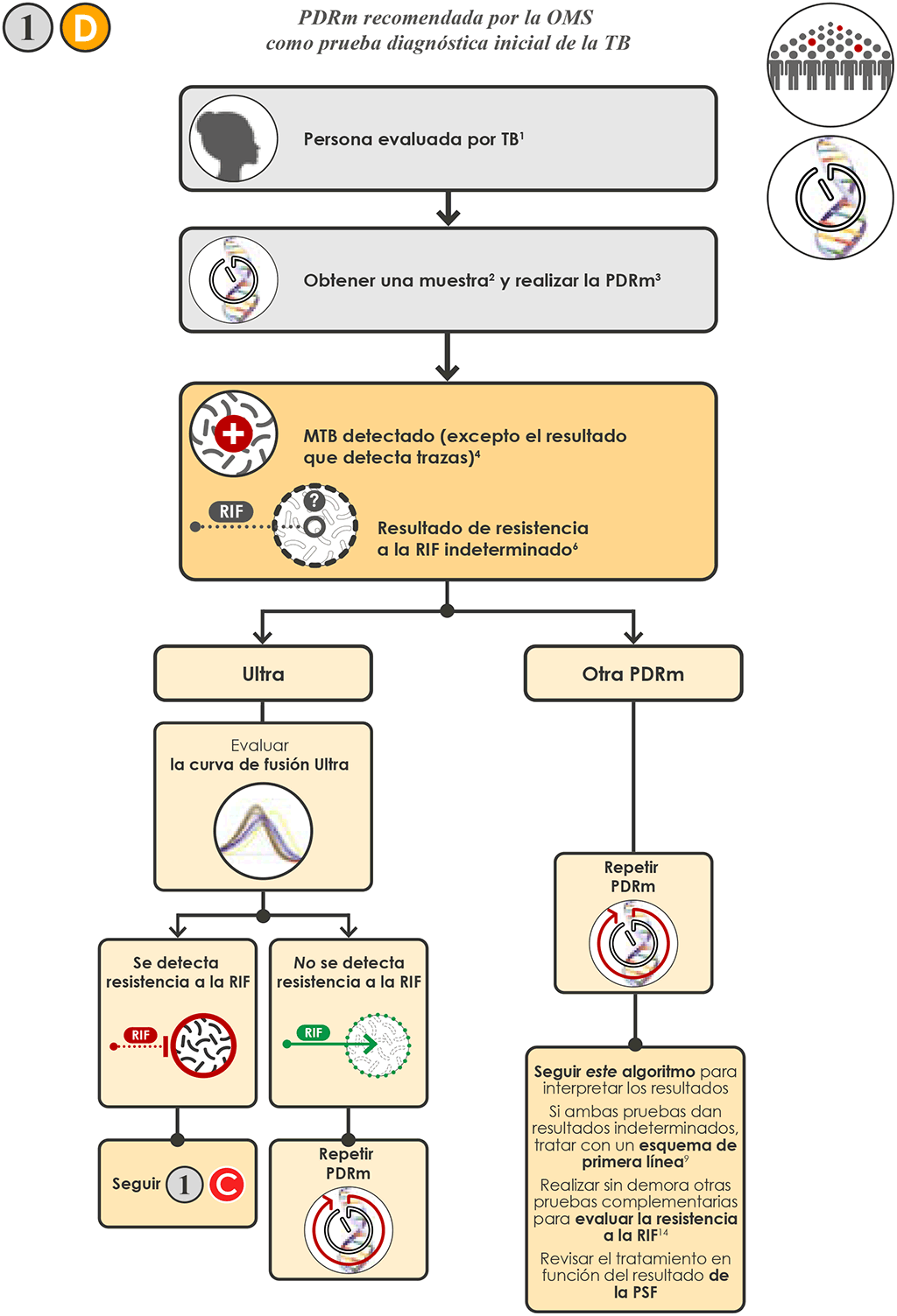
- Si el resultado de la PDRm es “MTB detectado, resistencia a la RIF indeterminada” 1 D, la interpretación y la prueba de seguimiento de la Xpert Ultra difiere de todas las demás PDRm (por ejemplo, Xpert MTB/RIF o Truenat MTB RIF Dx). Con cualquiera de las PDRm, el resultado inicial “MTB detectado” debe considerarse la confirmación bacteriológica de la TB. Se debe iniciar en el paciente un esquema apropiado con fármacos de primera línea contra la TB, de acuerdo con las directrices nacionales, a menos que el paciente tenga un riesgo alto de tener TB-MDR, en cuyo caso se debe iniciar un esquema de TB MDR. En la mayoría de los entornos, cuando se toman las decisiones terapéuticas los antecedentes de tratamiento contra la TB no son criterio suficiente para indicar un riesgo alto de tener TB MDR a fin de tomar decisiones sobre el tratamiento.
- Con la mayoría de las PDRm, un resultado “MTB detectado, resistencia a la RIF indeterminada” generalmente se debe a una muestra paucibacilar; en estos casos, es útil realizar de nuevo la prueba con una muestra fresca en el mismo centro.
- Si el resultado de la segunda PDRm es “MTB detectado, no se detecta resistencia a la RIF”, seguir al paso 3. Si el resultado es “MTB detectado, se detecta resistencia a la RIF”, seguir al paso 4.
- En algunos casos el resultado de la prueba con una segunda muestra, que también puede contener micobacterias escasas, es “MTB detectado, resistencia a la RIF indeterminada” o “MTB no detectado”. En estas situaciones, se pueden necesitar otras investigaciones complementarias como el cultivo y la PSF fenotípica para confirmar o excluir la resistencia a la RIF, porque el resultado indeterminado no suministra ninguna información sobre la resistencia.
- El resultado “MTB detectado ( excepto el resultado que detecta trazas), resistencia a la RIF indeterminada” obtenido con la prueba Xpert Ultra (sobre todo cuando el resultado semicuantitativo es alto o medio) puede deberse la presencia de deleciones grandes o mutaciones múltiples en la RDRR.
- Es necesario examinar de nuevo (de preferencia por un usuario de Xpert con experiencia o un supervisor) las curvas de fusión Ultra de las muestras con un resultado “MTB detectado (excepto el resultado que detecta trazas), resistencia a la RIF indeterminada”, revisando la amplificación de las sondas y el patrón de las curvas de fusión
- Las curvas de fusión que indican la presencia de una deleción grande o de mutaciones múltiples en la RDRR deben interpretarse “se detecta resistencia a la RIF”. En estos casos, seguir al paso 4.
- Si la curva de fusión no es indicativa de la presencia de una deleción grande ni de mutaciones múltiples en la RDRR, el resultado se interpreta como “indeterminado”. En estos casos, seguir al paso 5a para pruebas adicionales.
- Si el resultado semicuantitativo es alto o medio, puede ser útil la LPA-PL o la secuenciación del ADN.
- Es necesario examinar de nuevo (de preferencia por un usuario de Xpert con experiencia o un supervisor) las curvas de fusión Ultra de las muestras con un resultado “MTB detectado (excepto el resultado que detecta trazas), resistencia a la RIF indeterminada”, revisando la amplificación de las sondas y el patrón de las curvas de fusión
- Se pueden realizar el cultivo y PSF o la LPA-PL como pruebas de seguimiento para confirmar o excluir la resistencia a la RIF.
- Con la mayoría de las PDRm, un resultado “MTB detectado, resistencia a la RIF indeterminada” generalmente se debe a una muestra paucibacilar; en estos casos, es útil realizar de nuevo la prueba con una muestra fresca en el mismo centro.
- Si el resultado de la prueba Xpert Ultra es “MTB detectado, trazas” 1 E , se necesitan evaluaciones adicionales. Sin embargo, la OMS sugiere que no se repita la prueba Xpert Ultra con el fin de confirmar el resultado en los adultos con un resultado de trazas en la Xpert Ultra inicial.
- Revisar la valoración clínica con el fin de definir la edad de la persona, su situación con respecto a la infección por el VIH y los antecedentes de tratamiento contra la TB, y determinar si las muestras son pulmonares o extrapulmonares.
- En las personas con infección por el VIH se incluyen las personas positivas al VIH o cuya situación frente al VIH se desconoce, pero que presentan evidencia clínica fuerte de infección por el VIH en entornos donde hay una prevalencia alta de esta infección o en los miembros de grupos de riesgo de contraer el VIH. En todas las personas con situación desconocida frente al VIH, deben realizarse pruebas de detección del VIH, de acuerdo con las directrices nacionales
- Los niños se definen como menores de 15 años.
- Las personas con antecedentes recientes de tratamiento contra la TB incluyen las que completaron con éxito el esquema de tratamiento en los últimos 5 años. La probabilidad de un resultado positivo falso de una PDRm es más alta inmediatamente después de finalizar el tratamiento y disminuye lentamente con el transcurso del tiempo (7). Las personas que iniciaron el tratamiento sin completarlo y las personas con fracaso terapéutico se deben considerar con alto riesgo de tener TB-MDR; estos pacientes requieren una valoración clínica cuidadosa.
- Se recomienda utilizar la prueba Xpert Ultra con las muestras de LCR, ganglios linfáticos y de tejidos. Se dispone de pocos datos sobre el rendimiento de la prueba con otras muestras extrapulmonares.
- Los profesionales de la salud deben esforzarse por obtener antecedentes fiables sobre el tratamiento contra la TB y tener presente que algunos pacientes pueden no comunicar sus antecedentes de tratamiento debido a la estigmatización o la preocupación sobre la condición jurídica de los migrantes.
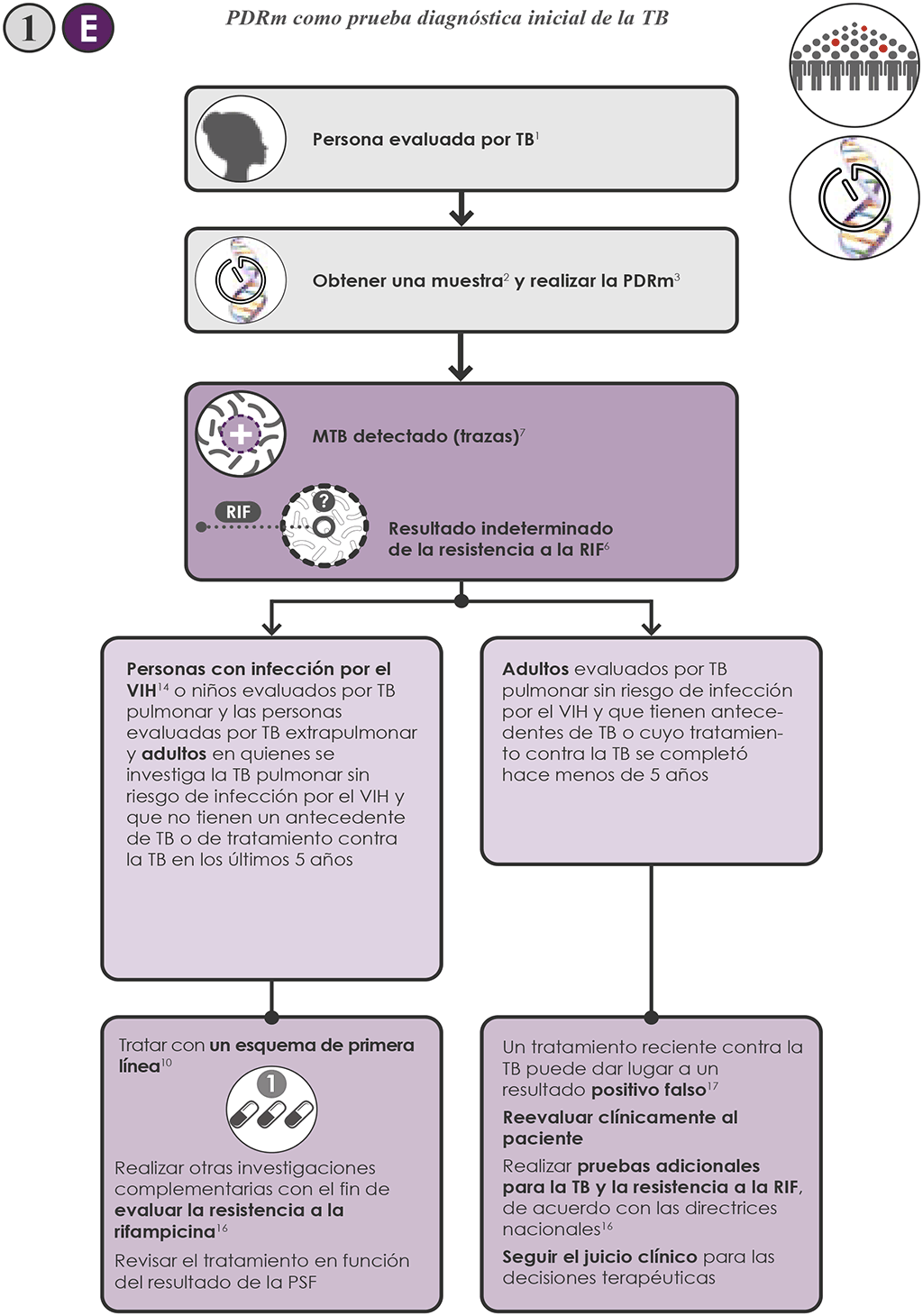
- En el caso de personas con infección por el VIH y niños evaluados por TB pulmonar; las personas evaluadas por TB extrapulmonar con muestras de LCR, ganglios linfáticos y tejidos; y los adultos evaluados por TB pulmonar sin riesgo de infección por el VIH y que no tienen antecedentes de tratamiento contra la TB en los últimos 5 años:
- Considerar el resultado “MTB detectado (trazas)”, obtenido con la primera muestra como la confirmación bacteriológica de la TB (es decir, un resultado positivo verdadero) y utilizarlo para las decisiones clínicas.
- Iniciar en el paciente un esquema contra la TB apropiado con los fármacos de primera línea, de acuerdo con las directrices nacionales, a menos que el paciente tenga un riesgo muy alto de tener TB-MDR, en cuyo caso se debe iniciar en estos pacientes un esquema para TB-MDR.
- Realizar otras investigaciones complementarias (por ejemplo, cultivo y PSF fenotípica) con el fin de confirmar o excluir la resistencia a la RIF.
- En el caso de los adultos evaluados por TB pulmonar sin riesgo de infección por el VIH y con antecedentes de tratamiento contra la TB en los últimos 5 años:
- En los adultos con antecedentes de tratamiento contra la TB reciente o con antecedentes de tratamiento desconocido, considerar que el resultado de trazas con la prueba Xpert Ultra puede ser un resultado positivo falso, debido a la presencia de bacilos no viables.
- Reevaluar clínicamente al paciente y realizar pruebas adicionales, de acuerdo con las directrices nacionales. Considerar la posibilidad de TB causada por reactivación, recaída o reinfección.
- Para iniciar el tratamiento, tener en cuenta el cuadro clínico inicial y el contexto del paciente. Tomar las decisiones clínicas teniendo en cuenta toda la información disponible y el juicio clínico.
- Otras investigaciones complementarias para detectar la TB pueden incluir la radiografía de tórax, valoraciones clínicas adicionales y la respuesta clínica a un tratamiento con antimicrobianos de amplio espectro (no deben usarse FQ).
- La repetición de la prueba Xpert Ultra es de utilidad incierta. Un reciente grupo de elaboración de directrices de la OMS recomendó que no se repita la prueba Xpert Ultra en las personas con un resultado de trazas de la prueba Xpert Ultra inicial para la detección del complejo M. tuberculosis.
- El cultivo y la PSF pueden ser útiles con el fin de detectar la TB y la farmacorresistencia. El resultado de trazas no aporta ninguna información sobre la resistencia a la RIF.
- Revisar la valoración clínica con el fin de definir la edad de la persona, su situación con respecto a la infección por el VIH y los antecedentes de tratamiento contra la TB, y determinar si las muestras son pulmonares o extrapulmonares.
- Si la prueba Xpert MTB no da ningún resultado 1 F o da un resultado de error o inválido, repetir la prueba Xpert MTB en el mismo centro de pruebas con una segunda muestra. Si el centro tiene a su disposición la LPA-PL y la segunda muestra tiene una baciloscopia positiva, se puede usar la LPA-PL para la repetición (aunque se prefiere repetir la prueba Xpert MTB porque su umbral de detección inferior al umbral de la LPA-PL).
Interpretación de los resultados discordantes
Este algoritmo se basa en el examen de una muestra con la PDRm para detectar el complejo M. tuberculosis y evaluar la sensibilidad a la RIF. En ocasiones se recomienda una prueba de seguimiento con el fin de garantizar que las decisiones clínicas estén bien fundamentadas. Sin embargo, puede haber resultados discordantes, sobre todo al comparar los resultados basados en el cultivo con resultados moleculares. Cada resultado discordante deberá investigarse caso por caso. A continuación se brindan algunas consideraciones generales en estos casos.
- Resultado de la PDRm “MTB detectado, excepto el resultado que detecta trazas” y cultivo negativo (véase el punto 5 para trazas).
- Debe haberse usado el resultado de la PDRm y el juicio clínico para orientar la decisión terapéutica, en espera de la prueba adicional.
- El resultado de la PDRm debe considerarse como la confirmación bacteriológica de la TB, si la muestra proviene de una persona que no había recibido tratamiento reciente con fármacos contra la TB. Los cultivos de personas con TB pulmonar pueden ser negativos por varias razones, incluido que el paciente esté recibiendo tratamiento contra la TB (un tratamiento eficaz elimina rápidamente la viabilidad del complejo M. tuberculosis), problemas de transporte o de procesamiento que inactivaron los bacilos de la TB, cultivos perdidos por contaminación, volumen inadecuado para la prueba o errores de laboratorio o de transcripción.
- Las medidas de seguimiento pueden incluir investigar de nuevo la TB en el paciente, examinar de nuevo la posibilidad de un tratamiento previo o actual con medicamentos contra la TB (incluido el uso de FQ), evaluar la respuesta al tratamiento y evaluar la posibilidad de un error de laboratorio o de transcripción.
- Resultado “MTB no detectado” en la PDRm y cultivo positivo.
- La decisión terapéutica debe basarse en el resultado del cultivo. Si el paciente comenzó el tratamiento basado en el juicio clínico, continuar el tratamiento. Registrar el paciente como un caso de TB confirmada bacteriológicamente.
- El resultado positivo del cultivo debe considerarse la confirmación bacteriológica de la TB porque el cultivo es el criterio de referencia actual para la confirmación de la TB en el laboratorio. Al usar una muestra de esputo, las PDR tienen una sensibilidad combinada de 83% a 90% para detectar la TB pulmonar, comparadas con el cultivo (28). Su sensibilidad es inferior en personas con infección por el VIH, los niños y otros tipos de muestras como el LCR.
- Los cultivos positivos falsos pueden ser consecuencia de una diversidad de causas como la contaminación cruzada en el laboratorio (por ejemplo, procesamiento inapropiado de muestras) o problemas de rotulación de las muestras. En los laboratorios que funcionan bien, estos errores son raros.
- Las medidas de seguimiento pueden incluir investigar de nuevo la TB en el paciente, realizar evaluaciones adicionales con PDR; cultivar muestras adicionales y evaluar la posibilidad de error del laboratorio o de transcripción. Si el paciente inició el tratamiento contra la TB con base en el juicio clínico, evaluar la respuesta al tratamiento.
- Resultado “MTB detectado, se detecta resistencia a la RIF” en la PDRm y sensible a la RIF en la PSF fenotípica.
- Usar el resultado de la PDRm para orientar las decisiones terapéuticas en espera de la prueba adicional.
- Se sabe que ciertas mutaciones generan resultados discordantes, sobre todo con el sistema BACTECTM con tubo indicador de crecimiento micobacteriano (MGITTM) (es decir, un resultado fenotípico sensible falso). El tratamiento de los pacientes infectados por cepas que albergan estas mutaciones a menudo fracasa con los esquemas de primera línea a base de RIF (26).
- En algunos entornos de prevalencia baja de TB MDR se han observado mutaciones silenciosas que generan un resultado falso de resistencia con PDR, pero esta situación es muy rara.
- Se han observado resultados falsos de resistencia a la RIF con el cartucho G4 de la prueba Xpert MTB/RIF, cuando el resultado de MTB detectado es “muy bajo”. La medida de seguimiento puede incluir una PDR a partir del cultivo.
- Las medidas de seguimiento pueden incluir secuenciación del ADN, LPA PL, PSF fenotípica con medios sólidos y evaluar la posibilidad de un error de laboratorio o de transcripción.
- Resultado “MTB detectado, no se detecta resistencia a la RIF” en la PDRm y resistente a la RIF en la PSF fenotípica.
- Debe modificarse el esquema de tratamiento en función de los resultados de la PSF fenotípica.
- Los resultados sensibles falsos frente a la RIF con PDRm son raros, pero se han observado en 1% a 5% de los casos de TB examinados con la prueba Xpert MTB/RIF en diversos entornos epidemiológicos. Se ha demostrado que las mutaciones localizadas en la región del gen rpoB que examina la prueba Xpert MTB explican de 95% a 99% de la resistencia a la RIF. El resto de la resistencia a la RIF surge por mutaciones fuera de la región examinada y dan lugar a un resultado “no se detecta resistencia a la RIF” en la prueba Xpert MTB.
- Las medidas de seguimiento pueden incluir secuenciación de ADN, repetición de la PSF fenotípica y evaluar la posibilidad de un error de laboratorio o de transcripción.
- Resultado “MTB detectado, trazas” en la prueba Xpert Ultra y cultivo negativo. En la interpretación de este resultado es necesario tener cuenta las características del paciente, el tipo de muestra y si la persona había recibido antes tratamiento contra la TB:
- Los cultivos pueden ser negativos por varias razones, incluido que el paciente esté recibiendo tratamiento contra la TB o con FQ, problemas de transporte o de procesamiento que inactivaron los bacilos de la TB, contaminación del cultivo o volumen inadecuado para la prueba o error de laboratorio o de transcripción.
- Las cantidades muy pequeñas de bacilos en una muestra que dan un resultado “MTB detectado, trazas” pueden deberse a la TB activa, una contaminación cruzada en el laboratorio, exposición reciente (o infección) a los bacilos de la TB (TB incipiente) y tratamiento actual o pasado contra la TB.
- El estudio multicéntrico de FIND mostró que muchas de las muestras que generaban resultados “MTB detectado, trazas” y cultivo negativo provenían de personas que habían completado el tratamiento en los últimos 4 a 5 años; muy probablemente debido a la presencia de escasos bacilos no viables o que no se multiplican. Por lo tanto, los resultados “MTB detectado, trazas” deben interpretarse en el contexto del tratamiento anterior.
- En el caso de personas con infección por el VIH y niños evaluados por TB pulmonar o cuando se examinan muestras extrapulmonares (LCR, ganglios linfáticos y tejidos), los beneficios de la mayor sensibilidad en la detección del complejo M. tuberculosis (es decir, positivos verdaderos) superan los daños eventuales de una especificidad reducida (es decir, positivos falsos).
- El resultado “MTB detectado, trazas” se considera como la confirmación bacteriológica de la TB (es decir, resultados positivos verdaderos) y en estos pacientes se debe haber iniciado el tratamiento, en función del resultado de la prueba Xpert Ultra. Considerar la probabilidad de que el resultado del cultivo haya sido un resultado negativo falso.
- Las medidas de seguimiento pueden incluir evaluar la respuesta al tratamiento (los resultados del cultivo no suelen estar disponibles antes de varias semanas después de la obtención de la muestra), examinar de nuevo la posibilidad de un tratamiento previo o actual con medicamentos contra la TB (incluido el uso de FQ) y examinar la posibilidad de un error de laboratorio o de transcripción.
- . En el caso de adultos evaluados por TB pulmonar sin riesgo de infección por el VIH, el equilibrio entre los beneficios y los daños posibles varía, dependiendo si la persona había recibido antes tratamiento contra la TB, debido a la especificidad reducida (es decir, positivos falsos).
- En las personas en quienes se puede excluir de manera fiable el tratamiento contra la TB actual o previo:
- Aunque el resultado “MTB detectado, trazas” debería considerarse como la confirmación bacteriológica de la TB (es decir, resultados positivos verdaderos), cualquier decisión clínica (por ejemplo, tratar por TB) debe tomarse teniendo en cuenta toda la información disponible de laboratorio, clínica y radiológica y el juicio clínico.
- Considerar la posibilidad de que el resultado del cultivo haya sido un resultado negativo falso, si las muestras provenían de una persona que no estaba recibiendo tratamiento con medicamentos contra la TB, debido al carácter paucibacilar de la muestra. Las medidas de seguimiento de los pacientes en quienes se inicia el tratamiento contra la TB pueden incluir investigar de nuevo la TB en el paciente, evaluar la respuesta al tratamiento, examinar de nuevo la eventualidad de un tratamiento anterior o actual con medicamentos contra la TB (incluido el uso de FQ), repetir la prueba Xpert Ultra, evaluar la posibilidad de un error de laboratorio o de transcripción y repetir el cultivo (de preferencia en medio líquido).
- En el caso de los adultos con un antecedente reciente de tratamiento contra la TB:
- Considerar la posibilidad de que el resultado “MTB detectado, trazas” de la prueba Xpert Ultra haya sido un resultado positivo falso, debido a la presencia de bacilos no viables. Un resultado negativo del cultivo concuerda con esta posibilidad.
- Si en estos pacientes se había iniciado el tratamiento contra la TB según el juicio clínico, las medidas de seguimiento pueden incluir: evaluar la respuesta al tratamiento, realizar pruebas adicionales de acuerdo con las directrices nacionales, repetir el cultivo (de preferencia en medio líquido) y evaluar la posibilidad de un error de laboratorio o de transcripción.
- En las personas en quienes se puede excluir de manera fiable el tratamiento contra la TB actual o previo:
3.1.2 Algoritmo 2: Prueba LAM-ICL como ayuda al diagnóstico de TB en las personas con infección por el VIH
El algoritmo 2 es el preferido para respaldar el diagnóstico de TB en las personas con infección por el VIH. Su aplicación es apropiada en los entornos con una carga alta de la infección por el VIH y en los pacientes con infección por el VIH que satisfacen los criterios de la prueba, sin tener en cuenta la carga general de la infección por el VIH. El algoritmo hace hincapié en la utilización de la LAM-ICL para detectar rápidamente a los pacientes que necesitan tratamiento contra la TB; también destaca que todas las personas con signos y síntomas de TB deben recibir una prueba molecular rápida (algoritmo 1). Es muy probable que los resultados de la LAM-ICL (duración de la prueba menos de 15 minutos) estén disponibles antes de los resultados de la PDRm y las decisiones terapéuticas deberían basarse en el resultado de la LAM-ICL, en espera de los resultados de otras pruebas diagnósticas.
La prueba LAM-ICL en orina disponible actualmente tiene una sensibilidad y especificidad suficientes para ayudar al diagnóstico de la TB en las personas coinfectadas por el VIH, pero su sensibilidad y especificidad son deficientes en las personas negativas frente al VIH. En consecuencia, en este algoritmo se hace hincapié en la utilización de la prueba LAM-ICL en orina como una prueba diagnóstica en todas las personas con infección por el VIH que presentan signos y síntomas de TB y también en otras situaciones específicas (que se describen a continuación) (11). Dada la sencillez de la LAM-ICL es apropiado implementarla fuera del laboratorio, por ejemplo, en los consultorios (sobre todo los consultorios que atienden personas con infección por el VIH en estado crítico), para un diagnóstico rápido de la TB e inicio oportuno del tratamiento, en los casos urgentes con presunción de TB y con infección por el VIH. El algoritmo 2a se utiliza en las personas con infección por el VIH evaluadas por TB (pulmonar o extrapulmonar) hospitalizadas y el algoritmo 2b se utiliza en personas con infección por el VIH evaluadas por TB (pulmonar o extrapulmonar) en atención ambulatoria Estos algoritmos son apropiados en los entornos tanto de carga alta como baja de TB-MDR. La elección de la prueba molecular puede ser diferente según el tipo de carga de TB-MDR. Por ejemplo, en un entorno con carga alta de TB-MDR sería preferible utilizar una PDRm que detecte de manera simultánea el complejo M. tuberculosis y la resistencia a la RIF (por ejemplo, la Xpert MTB/RIF), en lugar de una PDRm que requiera dos etapas para detectar la resistencia a la RIF.
 Reacción
Reacción