Enlaces transversales de Book para 6. Safety and management of adverse drug reactions in TB preventive treatment

Capítulo 6. Seguridad, manejo de las reacciones adversas y otros aspectos relacionados con los medicamentos en el tratamiento preventivo de la TB
La OMS ha recomendado durante mucho tiempo el uso del TPT en los grupos poblacionales en riesgo de contraer la TB, sobre todo en las personas con infección por el VIH y los contactos pediátricos en el hogar de pacientes con TB. Sin embargo, la ampliación programática del TPT ha permanecido limitada en la mayoría de los países con carga alta de TB e infección por el VIH, debido a otras prioridades concurrentes. Las preocupaciones con respecto a la eficacia y la seguridad del TPT y las interacciones con otros medicamentos, en especial los ARV, también pueden ser obstáculos a la ampliación programática. Otras cuestiones que se plantean con frecuencia se relacionan con la posibilidad de que el TPT aumente la resistencia a los medicamentos contra la TB en la comunidad y la duración de la protección del TPT contra la enfermedad o la mortalidad. En el presente capítulo se aborda la evidencia disponible en torno a algunos de estos aspectos importantes, con el objeto de facilitar la aceptación del TPT y su ampliación programática.
Seguridad de los medicamentos y reacciones adversas a los medicamentos
En general, es poco frecuente la aparición de eventos adversos graves que provoquen la muerte o que exijan el abandono del TPT. Sin embargo, es primordial detectar todo signo de toxicidad medicamentosa en etapa temprana y manejarla con firmeza, sobre todo en las personas que usualmente están sanas. Además del perjuicio que causan a la persona, estas eventualidades también pueden perjudicar la reputación del programa y provocar la suspensión del TPT en gran escala debido a la pérdida de confianza del público. Como ocurre con toda medida preventiva, el prestador de atención de salud debe sopesar los riesgos y los beneficios del TPT para cada persona. La realización de una anamnesis detallada y precisa (incluidos los medicamentos que se toman y las reacciones adversas a los medicamentos conocidas en el pasado) y el mantenimiento de una información actualizada en cada contacto con la persona que sigue el TPT, pueden ayudar a reconocer a las personas que precisan una vigilancia cuidadosa y el curso de acción más opiado si surge un evento adverso. También se debe realizar una supervisión periódica de las personas que reciben el TPT mediante consultas programadas (mensuales si es factible o según lo requiera la atención individual o los programas nacionales).
En el cuadro 6.1 se resumen los eventos adversos conocidos que se asocian con los fármacos utilizados en el TPT en la actualidad. Como parte del asesoramiento inicial, el trabajador de salud debe explicar la justificación del TPT, la importancia de completar el ciclo de tratamiento y hacer hincapié de nuevo en el riesgo asociado de TB activa. También se debe educar a la persona que recibe el TPT acerca de los eventos adversos probables e instarla a que se ponga en contacto con el prestador de atención sanitaria si aparecen eventos indicativos de toxicidad medicamentosa entre dos consultas (como pérdida del apetito, fatiga o debilidad persistente, malestar abdominal, náuseas, vómitos, orina de color oscuro, heces pálidas, erupción cutánea o prurito, coloración amarillenta en la piel o los ojos, hormigueo o adormecimiento en las manos o los pies). Si no se puede consultar a un trabajador de salud cuando aparecen estos síntomas, la persona que sigue el TPT debe suspenderlo de inmediato. Es necesario advertir con antelación a las personas tratadas con rifamicinas sobre la coloración rojiza de las secreciones debida a este medicamento.
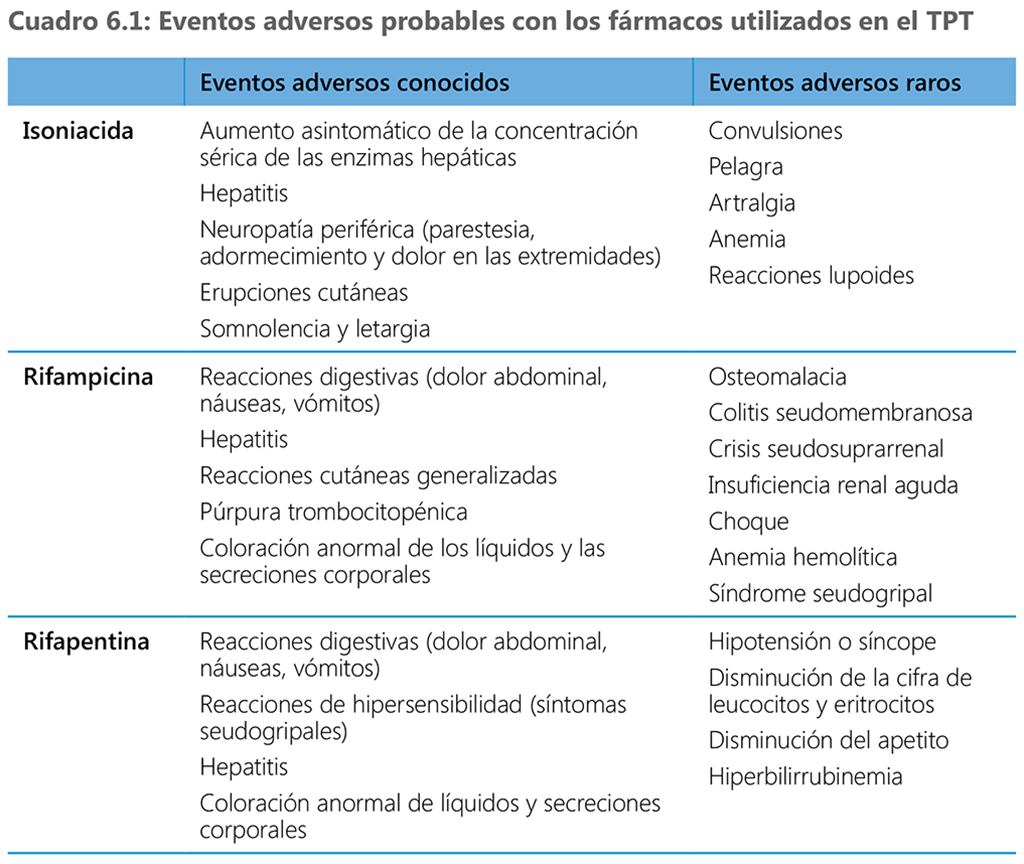
En los párrafos siguientes se examinan algunos de los eventos adversos asociados con los fármacos utilizados en el tratamiento preventivo y su manejo.
Isoniacida
- Aumento asintomático de las concentraciones séricas de las enzimas hepáticas que ocurre en 10% a 20% de las personas que toman isoniacida y que se suele normalizar incluso si se continúa el tratamiento. Sin embargo, en general se recomienda que se suspenda la isoniacida cuando las concentraciones de transaminasas exceden tres veces el límite superior normal y aparecen síntomas o cinco veces el límite superior normal, incluso en ausencia de síntomas.
- Hepatitis clínica que lleva a la muerte y ocurre en cerca de 0,1% de personas que toman isoniacida y es más frecuente cuando se combina con otros fármacos hepatotóxicos. Los factores que pueden aumentar la tasa de hepatitis o su gravedad incluyen el consumo diario de alcohol, una hepatopatía subyacente o el riesgo de hepatopatía, la edad por encima de 65 años y el uso concomitante de otros fármacos que se metabolizan en el hígado. La hepatitis sintomática es rara en personas menores de 20 años, aunque se han notificado casos graves y mortales. Los jóvenes con factores de riesgo subyacentes de hepatopatía se deben supervisar clínicamente con las mismas precauciones que las personas mayores.
- Neuropatía periférica (parestesia, adormecimiento y dolor de las extremidades> que ocurre en menos de 0,2% de las personas que toman isoniacida en dosis normales. Es más probable que aparezca en presencia de otras afecciones asociadas con neuropatías como la diabetes, la desnutrición, la infección por el VIH, la insuficiencia renal y el alcoholismo. El suplemento sistemático de piridoxina (vitamina B6) se recomienda solo en estas afecciones o cuando existen otros riesgos de toxicidad por isoniacida.
- La isoniacida es una causa secundaria conocida de pelagra. La isoniacida interrumpe la producción celular de niacina (vitamina B3) en las personas con carencia nutricional subyacente. La niacina desempeña una función vital en numerosos procesos metabólicos. La pelagra se diagnostica clínicamente por sus erupciones cutáneas características. Otros síntomas incluyen diarrea y cambios neuropsiquiátricos. Entre los grupos con un riesgo mayor de aparición de pelagra están las personas que consumen alcohol en exceso y las personas con una dieta no diversificada de alimentos básicos de maíz no enriquecidos.
- Otros efectos secundarios conocidos debidos a la isoniacida son erupción cutánea, somnolencia y letargo.
Rifampicina
- Síntomas digestivos, como náuseas, anorexia y dolor abdominal, que rara vez son lo suficientemente graves como para suspender el tratamiento.
- Hepatotoxicidad,que se manifiesta por hiperbilirrubinemia transitoria asintomática y puede presentarse en 0,6% de las personas que toman rifampicina. La hepatitis es más probable cuando la rifampicina se combina con isoniacida.
- Reacciones cutáneas,como prurito (con o sin erupción cutánea) pueden ocurrir en cerca de 6% de las personas que toman rifampicina. Estas reacciones suelen regresar espontáneamente y pueden no corresponder a una hipersensibilidad verdadera. Puede ser posible continuar el tratamiento
- Síndrome de hipersensibilidad a la rifamicina, que se ha comunicado en el pasado con el uso de rifampicina y se manifiesta por síntomas seudogripales. El síndrome, cuando ocurre, se presenta de manera característica unas pocas semanas después de haber iniciado el tratamiento y en la mayoría casos el tratamiento contra la TB se tolera posteriormente (96,97). En raras ocasiones, las rifamicinas se asocian con reacciones de hipersensibilidad con hipotensión, nefritis o trombocitopenia que se manifiestan por síntomas como fiebre, cefalea, mareo o vértigo, dolor osteomuscular, petequias y prurito.
- Coloración anaranjada de los líquidos y las secreciones corporales, que es previsible e inocua, pero es necesario alertar de antemano a las personas a quienes se recetan las rifamicinas.
Rifapentina
- En general, la rifapentina se asocia con un menor número de eventos adversos durante el TPT y es bien tolerada, incluso en personas con grados variables de disfunción hepática (98).
- Se han notificado reacciones medicamentosas sistémicas con significación clínica, en su mayoría seudogripales, hasta en 3,5% de las personas que reciben un esquema de 3HP y la mayor parte son leves y regresan en un plazo de 24 horas (99). Sin embargo, se justifica la supervisión clínica y la vigilancia continua de las reacciones sistémicas a los medicamentos. Aunque hay informes de personas que presentan hipotensión o síncope después de tomar el esquema Se han notificado reacciones medicamentosas sistémicas con significación clínica, en su mayoría seudogripales, hasta en 3,5% de las personas que reciben un esquema de 3HP y la mayor parte son leves y regresan en un plazo de 24 horas (99). Sin embargo, se justifica la supervisión clínica y la vigilancia continua de las reacciones sistémicas a los medicamentos. Aunque hay informes de personas que presentan hipotensión o síncope después de tomar el esquema de 3HP, los episodios de hipersensibilidad son en general poco frecuentes y suelen resolverse rápidamente después de suspender la medicación, sin ningún efecto a largo plazo.
- Otros efectos secundarios comunes incluyen el cambio en el color de los líquidos y las secreciones corporales a rojo anaranjado (benigno), efectos secundarios del aparato digestivo (como náuseas,vómitos, pérdida de apetito), disminución de las cifras de leucocitos y eritrocitos, erupción cutáneao prurito, dolor articular y ojos rojos (100).
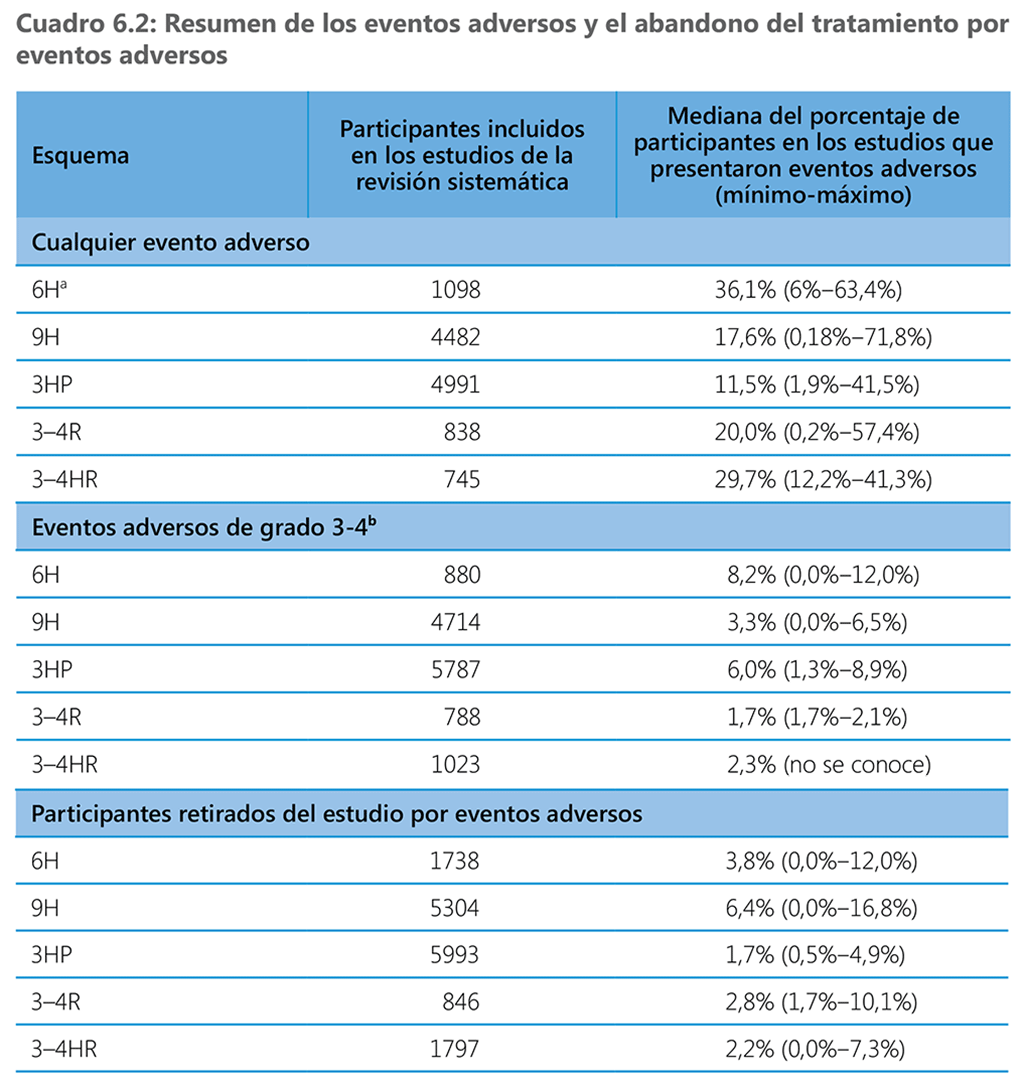
Un metanálisis de redes realizado en el 2014 (actualizado en el 2017) comparó los eventos adversos asociados con el uso de un esquema habitual de isoniacida con 3‑4R y 3‑4HR (45,101). Se encontró que los esquemas con rifampicina sola y rifampicina más isoniacida tenían un riesgo menor de hepatotoxicidad comparados con la monoterapia de isoniacida. Otra revisión sistemática que incluyó datos de 23 estudios aleatorizados y 55 no aleatorizados en el 2017 (102) notificó tasas altas de hepatotoxicidad con 6H o 9H (2%‑6%) y tasas más bajas con 3HP (1%) y 3‑4R (0,01%‑2%) (cuadro 6.2). Sin embargo, en esta revisión se señaló con claridad una documentación deficiente de los eventos adversos, heterogeneidad en los datos (diferentes definiciones de hepatotoxicidad) y un riesgo de sesgo alto en los estudios. Sin embargo, los datos aportaron indicios sobre la frecuencia de cualquier evento adverso y de eventos que eventualmente llevaban a la interrupción del tratamiento preventivo. Las medianas más altas de las tasas de abandono por eventos adversos se asociaron con 6H, seguido por 9H y las tasas más bajas con 3HP. Se comunicaron posibles reacciones de hipersensibilidad hasta en 4% de personas con 3HP y 2% con 3HR. Es menos común la comunicación de datos sobre defunciones por cualquier causa durante el TPT, pero en los estudios incluidos en el análisis no se comunicaron muertes en los participantes que recibieron 9H, 3HP y 3‑4R; sin embargo, ocurrieron algunas muertes en personas tratadas con 6H y 3‑4HR, la mayor parte de estudios en personas con infección por el VIH que no recibían TAR u otras afecciones concomitantes. Es tranquilizador que rara vez se comunicó anafilaxia con algún esquem.
En un estudio que comparaba la tolerabilidad de 3HP y 9H en personas seropositivas y seronegativas frente al VIH se encontraron tasas más altas de toxicidad de grado 3 y 4, hepatotoxicidad y eventos adversos graves en personas seropositivas al VIH que recibían 9H. Sin embargo, las personas con infección por el VIH presentaron tasas inferiores de episodios seudogripales o reacciones sistémicas a los medicamentos (1,0% contra 4,6%; p = 0,01) en comparación con las personas seronegativas (53).
 Reacción
Reacción